题目内容
17.为了适应市场的需求,超市里出售各种类型的食盐.如含碘盐、高钙盐、低钠盐等.低钠盐适合患有高血压、肾病、心脏病的患者服用,苹果酸钠盐(C4H5O5Na)是低钠盐的一种.请回答:(1)苹果酸钠盐含有4种元素,其相对分子质量是156.
(2)苹果酸钠盐分子中碳、氢元素的质量比为48:5.
(3)若某病人每天食用5.85g苹果酸钠盐,比食用相同质量的食盐(NaCl)少摄入钠元素多少克?(计算结果保留一位小数)
分析 (1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:根据苹果酸钠盐的化学式为C4H5O5Na,进行计算:
(1)苹果酸钠盐含有4种元素,根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得苹果酸钠盐的相对分子质量为:12×4+1×5+16×5+23=156.
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得苹果酸钠盐中各元素的质量比为(12×4):(1×5)=48:5.
(3)5.85gNaCl中钠元素的质量为:5.85g×$\frac{23}{23+35.5}$×l00%=2.3g;
5.85gC4H5O5Na中钠元素的质量为5.85g×$\frac{23}{156}$×100%≈0.86g;
5.85gC4H5O5Na比等质量的NaCl少的钠元素的质量为:2.3g-0.86g=1.4g.
故答案为:
(1)4;156;(2)48:5;(3)1.4g;
点评 本题难度不大,考查同学们灵活运用所学化学式的有关计算进行解题的能力.

练习册系列答案
相关题目
8.下列四个图象分别对应四种实验操作过程,其中正确的是( )
| A. | 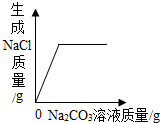 表示向一定质量的盐酸和氯化钙的混合溶液中逐滴加入碳酸钠溶液至过量 | |
| B. | 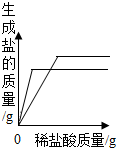 表示向等质量的镁和锌中分别滴加稀盐酸至过量 | |
| C. | 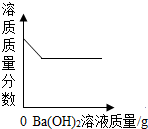 表示向一定质量的稀硫酸中逐滴加入氢氧化钡溶液至过量 | |
| D. | 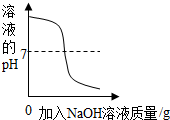 表示向一定体积的稀盐酸中逐滴加入氢氧化钠溶液 |
12.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 碱溶液能跟某些非金属氧化物反应,所以碱溶液能吸收CO气体 | |
| B. | 中和反应生成盐和水,所以有盐和水生成的反应一定是中和反应 | |
| C. | 碳酸盐能与酸反应产生气体,所以能与酸反应产生气体的一定是碳酸盐 | |
| D. | 酸性溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的一定是酸性溶液 |
2.大自然中学的煊煊同学取未完全锈蚀的铁丝样品,称量其质量为21.6g,待其完全锈蚀后质量变为24g,则煊煊所取样品中的铁粉的质量分数为(假设铁锈的化学式为Fe2O3)( )
| A. | 33.3% | B. | 66.7% | C. | 56% | D. | 46.7% |
3.“低碳生活”、“低碳经济”、“碳减排”等日常出现在电视新闻或报纸上,其中关于“低碳生活”中的“低碳”是指( )
| A. | 生活中不用含碳的物质 | B. | 较低的二氧化碳排放 | ||
| C. | 停止含碳矿物的开采和加工 | D. | 禁止使用煤炭、石油 |
20.下列说法中,错误的是( )
| A. | 盐溶液不一定呈中性 | |
| B. | 碱的组成中一定含有“OH”原子团 | |
| C. | 物质溶于水时一定伴随着吸热和放热两个过程 | |
| D. | 中和反应的实质是H+离子与OH-离子反应生成H2O |
1.在氮的氧化物中,测得氮、氧两种元素的质量比为7:12,则该氧化物是( )
| A. | N2O5 | B. | N2O3 | C. | N2O | D. | NO2 |
 将KOH和Ca(OH)2混合物1.86g全部溶于一定量水中形成稀溶液,再缓缓通入足量的CO2气体.当生成沉淀的质量刚好最大时,消耗CO2的体积为224mL[已知该条件下CO2的密度为(44÷22.4)g/l,忽略CO2溶于水情况.已知CaCO3+H2O+CO2=Ca(HCO3)2]CO2+Ca(OH)2=CaCO3↓+H2O
将KOH和Ca(OH)2混合物1.86g全部溶于一定量水中形成稀溶液,再缓缓通入足量的CO2气体.当生成沉淀的质量刚好最大时,消耗CO2的体积为224mL[已知该条件下CO2的密度为(44÷22.4)g/l,忽略CO2溶于水情况.已知CaCO3+H2O+CO2=Ca(HCO3)2]CO2+Ca(OH)2=CaCO3↓+H2O