题目内容
13.实验室欲用含杂质的粗盐配制50g 5%的NaCl溶液,用如图甲实验操作可完成两个实验.甲实验是除去粗盐中难溶性杂质,乙实验为配制50g溶质的质量分数为5%的氯化钠溶液.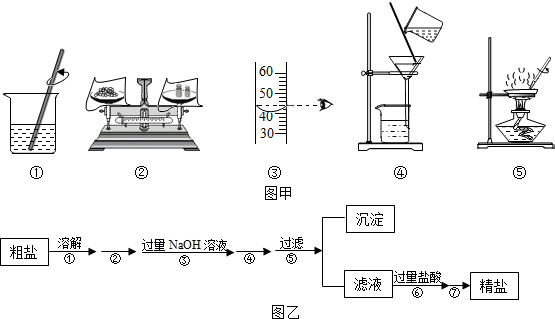
回答下列问题
(1)甲实验的步骤为①④⑤(填序号),
(2)乙实验若按照②③①的步骤进行操作,则配制的氯化钠溶液溶质的质量分数偏大(填“偏大”“偏小”“不变”)
(3)经过甲实验提纯后的食盐还含有少量Na2SO4,MgCl2,CaCl2等可溶性杂质,某实验小组利用化学实验室常用仪器对粗盐样品进一步提纯,提纯步骤如图乙,请根据实验步骤回答下列问题:
1.请写出实验步骤②和④中所加的试剂依次为过量BaCl2溶液、过量Na2CO3溶液.
2.步骤⑥中加入过量盐酸的目的是除去过量的氢氧化钠和碳酸钠.
3.写出步骤③所涉及的反应方程式2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
分析 (1)根据粗盐提纯的主要步骤是溶解、过滤、蒸发进行分析;
(2)根据溶质质量分数等于溶质质量和溶液质量的比进行分析;
(3)1、根据食盐还含有少量Na2SO4,MgCl2,CaCl2等可溶性杂质进行分析;
2、根据加入的氢氧化钠和碳酸钠是过量的进行分析;
3、根据氢氧化钠和氯化镁生成氢氧化镁沉淀和氯化钠进行分析.
解答 解:(1)粗盐提纯的主要步骤是溶解、过滤、蒸发,所以甲实验的步骤为①④⑤;
(2)配制一定质量分数的溶液的步骤:计算、称量(量取)、溶解,乙实验按照②③①的步骤进行操作,③中量取的水的体积偏小,则配制的溶液浓度偏大;
(3)1、实验步骤②是除去硫酸钠,步骤④是除去氯化钙,所以所加的试剂依次为过量 BaCl2 溶液,过量Na2CO3溶液;
2、加入的氢氧化钠和碳酸钠是过量的,所以步骤⑥中加入过量盐酸的目的是除去过量的氢氧化钠和碳酸钠;
3、氢氧化钠和氯化镁生成氢氧化镁沉淀和氯化钠,化学方程式为:2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
故答案为:(1)①④⑤;
(2)偏大;
(3)1、过量 BaCl2 溶液,过量Na2CO3溶液;
2、除去过量的氢氧化钠和碳酸钠;
3、2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
点评 本题难度不大,掌握粗盐提纯的步骤与注意事项、配制一定质量分数的溶液的步骤与注意事项是正确解答本题的关键.

练习册系列答案
相关题目
3.“低碳生活”、“低碳经济”、“碳减排”等日常出现在电视新闻或报纸上,其中关于“低碳生活”中的“低碳”是指( )
| A. | 生活中不用含碳的物质 | B. | 较低的二氧化碳排放 | ||
| C. | 停止含碳矿物的开采和加工 | D. | 禁止使用煤炭、石油 |
4.以下净化水的过程,属于化学变化的是( )
| A. | 煮沸 | B. | 过滤 | C. | 吸附 | D. | 消毒 |
1.在氮的氧化物中,测得氮、氧两种元素的质量比为7:12,则该氧化物是( )
| A. | N2O5 | B. | N2O3 | C. | N2O | D. | NO2 |
18.下列实验设计能达到目的是( )
| 选项 | A | B | C | D |
| 实验设计 |  | 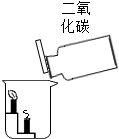 | 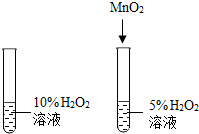 | 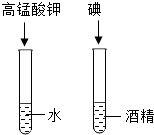 |
| 实验目的 | 证明二氧化碳与水反应生成碳酸 | 证明二氧化碳一般不可燃、不助燃、密度大于空气 | 证明二氧化锰是过氧化氢分解的催化剂 | 证明同一物质在不同溶剂中的溶解性不同 |
| A. | A | B. | B | C. | C | D. | D |
2.小明在实验室过滤某种液体,他不需要的仪器是( )
| A. | 烧杯 | B. | 漏斗 | C. | 酒精灯 | D. | 玻璃棒 |
3.下列叙述中不正确的是( )
| A. | 铝制品比铁制品耐锈蚀的原理:铁的化学性质比铝活泼 | |
| B. | 用汽油洗涤衣服上的油渍的原理:油渍易溶于汽油 | |
| C. | 用含Mg(OH)2的药物治疗胃酸过多的原理:胃酸能和Mg(OH)2发生中和反应 | |
| D. | 食醋除水垢的原理:食醋中的醋酸与水垢发生化学反应,生成可溶于水的物质 |
