题目内容
14.碘盐是在食盐中添加了一定量的碘酸钾(KIO3),碘酸钾中I元素的质量分数为59.3%(精确到0.1%),碘酸钾中碘元素的化合价为+5.防辐射最有效的措施是每天摄入碘100mg.经化验某品牌的加碘盐每1000g中含有碘元素50mg.若我们每天只食用加碘盐来防治核辐射,则要食用此加碘盐2000g.所以每天加碘盐防治核辐射不合理(填“合理”或“不合理”).分析 物质中某元素的质量分数=$\frac{原子的相对原子质量×原子个数}{相对分子质量}$×100%,在化合物中,元素化合价的代数和为零,根据这一原则可以求出碘酸钾中的碘元素的化合价;通过计算可知,我们每天只食用加碘盐来防治核辐射,则要食用此加碘盐2000g,这是不可能的
解答 解:碘酸钾中碘元素的质量分数是$\frac{127}{39+127+16×3}$×100%≈59.3%.
根据在化合物中正负化合价代数和为零计算,KIO3中碘(I)的化合价为 (+1)+x+(-2)×3=0,则x=+5;
加碘盐每1000g中含有碘元素50mg,我们每天只食用加碘盐来防治核辐射,则要食用此加碘盐100mg×$\frac{1000g}{50mg}$=2000g.因为每个人每天食用的食盐不可能达到2000g,所以不能靠食用碘盐防治核辐射.
故答案为:59.3%;+5;2000;不合理.
点评 本题主要考查化合价的求法、相关方面的计算,要根据化合物中元素化合价代数和为零的原则求某种元素的化合价.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
9.对物质进行归类整理时化学学习的一种重要方法,下列归类关系相符的是( )
| A. | 蒸馏水-氧化物 | B. | 天然气-纯净物 | C. | 纯碱-碱 | D. | 碳酸氢钠-酸 |
10.鉴别空气、氧气和二氧化碳3瓶气体最合理的方法是( )
| A. | 闻气味 | B. | 将集气瓶倒扣在水中 | ||
| C. | 观察颜色 | D. | 将燃着的木条伸入集气瓶中 |
2.“对比实验”是科学探究中常用的一种方法,以下实验没有体现“对比”的是( )
| A. |  FeCl3和CuSO4对H2O2分解的催化效果 | |
| B. |  测定空气中氧气含量 | |
| C. |  探究微粒运动 | |
| D. |  探究铁片锈蚀条件 |
19.化学在生活中有广泛的应用,下列做法或说法中错误的是( )
| A. | 回收废旧电池,既可节约金属资源又可减少环境污染 | |
| B. | 用灼烧的方法区别棉花和羊毛 | |
| C. | 微量元素是人体必需的营养素,多吃无害 | |
| D. | 使用可降解塑料代替传统塑料,有利于减轻“白色污染” |
6.类推是学习化学的一种重要方法,以下类推正确的是( )
| A. | 有机物中都含有碳元素,则含有碳元素的化合物都是有机物 | |
| B. | 溶液中有晶体析出,其溶质的质量减小,则溶质的质量分数一定减小 | |
| C. | 碱性溶液能使酚酞试液变红,则滴入酚酞试液后变红的溶液一定呈碱性 | |
| D. | 碳酸盐与酸反应有气泡产生,则与酸反应有气泡产生的物质一定是碳酸盐 |
3.甲和乙在一定条件下反应生成丙和丁,结合微观示意图分析,下列结论不正确的是( )
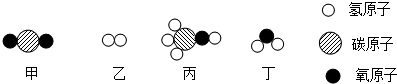

| A. | 发生反应的甲和乙的质量比为22:3 | B. | 生成物丙和丁均为氧化物 | ||
| C. | 生成的丙和丁的分子个数比为1:1 | D. | 反应前后原子总数不变 |