题目内容
20.实验室用20.0克过氧化氢溶液和1.0克二氧化锰制取氧气,实验的相关数据如下表:| 气体发生装置内物质的总质量 | |
| 反应前 | 21.0g |
| 反应后 | 20.2g |
(2)反应生成氧气的质量为0.8g.
(3)计算参加反应的过氧化氢的质量(写出必要的计算过程).
分析 (1)根据二氧化锰是该反应的催化剂,化学反应前后质量不变进行分析;
(2)根据质量守恒定律进行分析;
(3)根据化学方程式和计算参加反应的过氧化氢的质量.
解答 解:(1)二氧化锰是该反应的催化剂,化学反应前后质量不变,所以反应结束后过滤、烘干,得到滤渣的质量为1.0g;
(2)反应生成氧气的质量为:21.0g-20.2g=0.8g;
(3)生成参加反应的过氧化氢的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 0.8g
$\frac{68}{x}$=$\frac{32}{0.8g}$
x=1.7g
故答案为:(1)1.0g;
(2)0.8g;
(3)1.7g.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
11.二氧化氮是大气的污染物之一.煤燃烧会产生一部分二氧化氮气体,它会与空气中的氧气、水蒸气发生反应形成酸雨,NO2+O2+H2O═HNO3,配平后各物质的化学计量数分别是( )
| A. | 1,1,1,2 | B. | 2,1,1,2 | C. | 4,1,2,4 | D. | 6,2,3,6 |
8.某校兴趣小组的同学在综合实践活动中,从水泥厂拿来一块石灰石样品,技术员告诉他们此样品中含有的杂质是二氧化硅,二氧化硅难溶于水,不能与盐酸反应.为了测定该石灰石的纯度,兴趣小组的同学取用8.00g这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸100克分5次加入,充分反应后,经过滤、干燥等操作后称量,得到如下数据:
试回答下列问题:
(l)表中m的值为4g.杂质的质量是1.2g
(2)计算该石灰石样品的纯度.
(3)反应生成的气体质量是多少克?
| 实 验 次 数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸的质量/g | 20.0 | 20.0 | 20.0 | 20.0 | 20.0 |
| 剩余固体的质量/g | 6.00 | m | 2.00 | 1.20 | 1.20 |
(l)表中m的值为4g.杂质的质量是1.2g
(2)计算该石灰石样品的纯度.
(3)反应生成的气体质量是多少克?
15.①酸雨②可吸入颗粒物③空气中一氧化碳含量增加都会对环境造成污染,其中由煤和石油等化石燃料燃烧造成的是( )
| A. | ①②③ | B. | ①③ | C. | ②③ | D. | ①② |
5.下列实验操作能达到目的是( )
| A. | 向滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,则证明BaCl2有酸性 | |
| B. | 准确称取14.80g Ca(OH)2,配制50g 29.6%的Ca(OH)2溶液 | |
| C. | 在实验室,可无需查阅资料用98%的浓硫酸来配制50g 20%的硫酸溶液 | |
| D. | 测定溶液的pH,先用水润湿pH试纸,然后将试纸插入待测液中 |
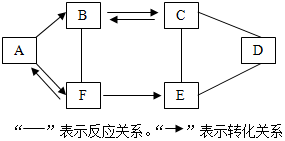 A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示.己知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质.(部分反应物、生成物及反应条件
A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示.己知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质.(部分反应物、生成物及反应条件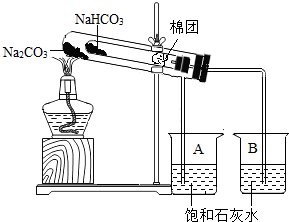 某校化学兴趣小组对苏打(Na2CO3)和小苏打(NaHCO3)在生活中具有何作用,如何鉴别苏打和小苏打进行了如下的探究实验活动,请你参与他们的探究过程,并回答相关问题:
某校化学兴趣小组对苏打(Na2CO3)和小苏打(NaHCO3)在生活中具有何作用,如何鉴别苏打和小苏打进行了如下的探究实验活动,请你参与他们的探究过程,并回答相关问题: