题目内容
15.将100g氯酸钾与20g二氧化锰混合加热,反应一会儿停止加热,称得剩余固体质量为100.8g.求参加反应的氯酸钾的质量?(K:39 Cl:35.5 O:16)分析 根据质量守恒定律,生成氧气的质量=反应前物质质量总和-反应后物质质量总和;利用氯酸钾受热分解的化学方程式和生成氧气的质量,列出比例式,就可计算出参与反应的氯酸钾质量.
解答 解:根据质量守恒定律,生成氧气的质量=100g+20g-100.8g=19.2g;
设参与反应的氯酸钾质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 19.2g
$\frac{245}{x}=\frac{96}{19.2g}$
x=49g
答:参加反应的氯酸钾的质量为49g.
点评 本题主要考查学生利用化学方程式和质量守恒定律解答问题的能力.解题的关键是根据质量守恒定律求出生成氧气的质量.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
20.空气的净化越来越受到人们的关注.下列气体中,属于空气污染物的是( )
| A. | 二氧化硫 | B. | 二氧化碳 | C. | 氮气 | D. | 氧气 |
6.下列物质长期放置在敞口容器中,质量增加且会变质的是( )
| A. | 氢氧化钠固体 | B. | 浓盐酸 | C. | 浓硫酸 | D. | 浓硝酸 |
3.2011年4月7日,甘肃省平凉市崆峒区发生一起疑似食物中毒事件,中毒病例均服用过散装牛奶,确认系亚硝酸盐中毒.生活中常有发生亚硝酸钠中毒事件的报道,这是因为亚硝酸钠外观酷似食盐且有咸味;工业用盐中常混有亚硝酸钠,有关氯化钠和亚硝酸钠的部分资料如下表:如要检验食盐中有无亚硝酸钠,下列判定方法错误的是( )
| 化学式 | 水溶性 | 酸碱性 | 热稳定性 | 和稀盐酸作用 |
| NaNO2 | 100℃时的溶解度为163克 | 若碱性 | 320℃以上会分解放出刺激性气体 | 放出红棕色气体 |
| NaCl | 100℃时的溶解度为39.12克 | 中性 | 受热不分解 | 不反应 |
| A. | 在食盐中加人盐酸,观察有无红棕色气体放出 | |
| B. | 蒸干100克100℃食盐饱和溶液,称量溶质的质量是不是39.12克 | |
| C. | 用pH试纸测定食盐溶液的酸碱性 | |
| D. | 把食盐加热到3200C以上观察有无刺激性气体放出 |
10.2008年9月曝光的“结石宝宝”事件,与婴幼儿服用含有三聚氰胺(C3H6N6)的奶粉有关.下列关于三聚氰胺的说法,错误的是( )
| A. | 含有三聚氰胺的奶粉是混合物 | B. | 三聚氰胺是一种无机物 | ||
| C. | 三聚氰胺由C、H、N三种元素组成 | D. | 三聚氰胺的式量是126 |
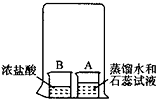 在烧杯A中装入20mL蒸馏水,滴入2~3滴石蕊试液;在烧杯B中装入10mL浓盐酸,然后用一只大烧杯把A、B两烧杯溶液罩在一起(如图所示).过几分钟后,可以观察到烧杯A中液体变成红色.请写出由该实验可知(浓)盐酸具有的一条性质:易挥发.
在烧杯A中装入20mL蒸馏水,滴入2~3滴石蕊试液;在烧杯B中装入10mL浓盐酸,然后用一只大烧杯把A、B两烧杯溶液罩在一起(如图所示).过几分钟后,可以观察到烧杯A中液体变成红色.请写出由该实验可知(浓)盐酸具有的一条性质:易挥发. 铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入氧化铁和铝粉的混合物,用镁条引燃发生反应,反应的化学方程式为:Fe2O3+2Al $\frac{\underline{\;点燃\;}}{\;}$ Al2O3+2Fe.有关该反应的下列说法中,该反应属于( )
铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入氧化铁和铝粉的混合物,用镁条引燃发生反应,反应的化学方程式为:Fe2O3+2Al $\frac{\underline{\;点燃\;}}{\;}$ Al2O3+2Fe.有关该反应的下列说法中,该反应属于( )