题目内容
20.写出下列溶液中溶质的化学式.盐酸HCl;石灰水Ca(OH)2;碳酸饮料H2CO3;食盐水NaCl;
稀硫酸与硫酸铜混合液中加入过量铁粉,充分反应后,过滤,滤液中的溶质FeSO4.
分析 根据溶液中溶质和溶剂的判断方法(即气体、固体溶于液体中,液体是溶剂,气体、固体为溶质;液体和液体相溶时,量多的为溶剂,量少的为溶质;有水时,不管量多量少,一般把水看作溶剂;没有指明溶剂时,常把水看作溶剂),逐一分析判断即可.
解答 解:盐酸是氯化氢气体的水溶液,氯化氢气体是溶质,其化学式为:HCl.
石灰水是氢氧化钙的水溶液,氢氧化钙是溶质,其化学式为:Ca(OH)2.
碳酸饮料中碳酸是溶质,其化学式为:H2CO3.
食盐水是氯化钠的水溶液,氯化钠是溶质,其化学式为:NaCl.
稀硫酸与硫酸铜混合液中加入过量铁粉,铁与稀硫酸反应生成硫酸亚铁溶液和氢气,与硫酸铜溶液反应生成硫酸亚铁溶液和铜,充分反应后,过滤,所得滤液为硫酸亚铁溶液,溶质是硫酸亚铁,其化学式为:FeSO4.
故答案为:HCl;Ca(OH)2;H2CO3;NaCl;FeSO4.
点评 本题难度不大,主要考查了溶液中溶质和溶剂的判断,掌握常见溶液的组成是正确解答此类题的关键所在.

练习册系列答案
相关题目
5.下列四种微粒中,具有相似的化学性质的是( )


| A. | ②③ | B. | ①④ | C. | ②④ | D. | ①② |
11.下列反应中,属于复分解反应的是( )
| A. | CO2+H2O═H2CO3 | B. | HCl+AgNO3═HNO3+AgCl↓ | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ |
8.为测定其真实的含钙量,孙东同学每次取10片钙片放入已称量的含足量盐酸的烧杯中,钙片中除CaCO3 外,其它成分不与HCl反应.充分反应后再称取烧杯和剩余物的总质量.孙东同学做了三次实验,数据如表:
请列式计算每片这样的钙片含碳酸钙的质量.
| 物质的质量 | 第一次 | 第二次 | 第三次 | 平均值 |
| 反应前;烧杯+盐酸 | 22g | 22g | 22g | 22g |
| 10片钙片 | 8g | 8g | 8g | 8g |
| 反应后;烧杯+剩余物 | 26.7g | 26.5g | 26.9g | 26.7g |
12.下列有关化学反应类型的判断;错误的是( )
| A. | SO3+H2O═H2SO4 化合反应 | |
| B. | NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑分解反应 | |
| C. | 2Al+WO3$\frac{\underline{\;高温\;}}{\;}$Al2O3+W置换反应 | |
| D. | 6CO2+6H2O$\frac{\underline{\;\;\;光照\;\;\;}}{叶绿素}$C6H12O6+6O2 复分解反应 |
9.下列图象不能正确反映对应变化关系的是( )
| A. | 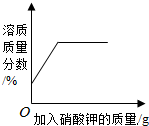 20℃时,向一定量的硝酸钾不饱和溶液中加入硝酸钾固体 | |
| B. | 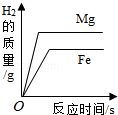 将等质量的镁片和铁片投入到足量稀硫酸中 | |
| C. | 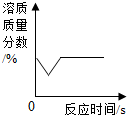 向某温度下一定量的熟石灰饱和溶液中加入少量生石灰 | |
| D. | 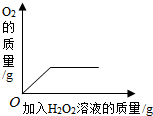 向盛有少量二氧化锰的烧杯中不断地加入过氧化氢溶液 |