题目内容
15.现有下列实验装置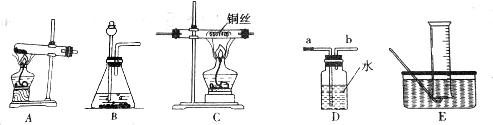
为了测定某高锰酸钾样品的纯度(假设杂质受热不反应且不升华),我校化学兴趣小组的同学准备选用上述部分装置来完成测定任务
(1)小华选用装置A、E完成了实验,该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,用E装置收集氧气的时机是气泡均匀连续放出时;
(2)经过仔细分析,小聪同学认为小华的测定结果偏大.原因是收集的氧气中混入了水蒸气;
(3)小聪只选用一种装置就测定出了准确的结果.需要测量的数据有高锰酸钾样品质量和反应后试管中所剩固体物质的总质量.
分析 (1)根据用高锰酸钾制取氧气的反应、注意事项分析回答;
(2)根据用排水法收集氧气时易混入水蒸气分析;
(3)根据高锰酸钾分解放出了氧气的质量可以求出高锰酸钾的质量,据此分析需要测量的数据.
解答 解:(1)小华选用装置A、E完成了实验,该反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,用E装置收集氧气的时机是气泡均匀连续放出时;
(2)经过仔细分析,小聪同学认为小华的测定结果偏大.原因是收集的氧气中混入了水蒸气;
(3)由于高锰酸钾分解放出了氧气,根据氧气的质量就可以求出高锰酸钾的质量,小聪只选用一种装置就测定出了准确的结果.需要测量的数据有:高锰酸钾样品质量和反应后试管中所剩固体物质的总质量.
故答为:(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,气泡均匀连续放出时;(2)收集的氧气中混入了水蒸气;(3)高锰酸钾样品质量和反应后试管中所剩固体物质的总质量.
点评 本题的难度不大,了解实验室用高锰酸钾制取氧气的原理、装置、注意事项等知识即可分析解答.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目

 如图所示为某种加钙食盐包装标签上的部分文字.请仔细阅读后回答以下问题:
如图所示为某种加钙食盐包装标签上的部分文字.请仔细阅读后回答以下问题:
 某兴趣小组为测定提纯后的碳酸钠的含量,进行如下实验:
某兴趣小组为测定提纯后的碳酸钠的含量,进行如下实验: 如图是初中化学中常见物质间的转化关系,图中“→”表示转化关系,“-”表示相互能反应,反应条件间和部分物质已省略.已知A是胃酸的主要成分,D可用于配置波尔多液,其中A+B→C+F+G,A+N→C+F+G,请回答下列问题.
如图是初中化学中常见物质间的转化关系,图中“→”表示转化关系,“-”表示相互能反应,反应条件间和部分物质已省略.已知A是胃酸的主要成分,D可用于配置波尔多液,其中A+B→C+F+G,A+N→C+F+G,请回答下列问题.