题目内容
20. 如图是初中化学中常见物质间的转化关系,图中“→”表示转化关系,“-”表示相互能反应,反应条件间和部分物质已省略.已知A是胃酸的主要成分,D可用于配置波尔多液,其中A+B→C+F+G,A+N→C+F+G,请回答下列问题.
如图是初中化学中常见物质间的转化关系,图中“→”表示转化关系,“-”表示相互能反应,反应条件间和部分物质已省略.已知A是胃酸的主要成分,D可用于配置波尔多液,其中A+B→C+F+G,A+N→C+F+G,请回答下列问题.(1)写出A的化学式HCl;N的一种用途制取洗涤剂、制玻璃的原料;
(2)写出D→E的化学方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(3)写出A-N的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
分析 根据题目中的突破口“A是胃酸的主要成分”,可推测A为稀盐酸;根据“D可用于配置波尔多液”,可推测D为硫酸铜或氢氧化钙,根据“A+B→C+F+G,A+N→C+F+G”,结合图框,可推测D只能为氢氧化钙,则推测A与碳酸钠、碳酸氢钠反应,依次为突破口,结合图框,可推测:A为稀盐酸,B为碳酸氢钠,C为氯化钠,D为氢氧化钙,E为氢氧化钠,F为为水,G为二氧化碳,M为碳酸钙,N为碳酸钠.带入检验,符合题意.
解答 解:
根据题目中的突破口“A是胃酸的主要成分”,可推测A为稀盐酸;根据“D可用于配置波尔多液”,可推测D为硫酸铜或氢氧化钙,根据“A+B→C+F+G,A+N→C+F+G”,结合图框,可推测D只能为氢氧化钙,则推测A与碳酸钠、碳酸氢钠反应,依次为突破口,结合图框,可推测:A为稀盐酸,B为碳酸氢钠,C为氯化钠,D为氢氧化钙,E为氢氧化钠,F为为水,G为二氧化碳,M为碳酸钙,N为碳酸钠.带入检验,符合题意.
(1)根据分析,A的化学式为HCl;N的一种用途制取洗涤剂、制玻璃的原料;
(2)根据分析,D→E即氢氧化钙与碳酸钠溶液反应,其化学方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(3)根据分析,A-N即稀盐酸与碳酸钙反应,其化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
故答案为:
(1)HCl;制取洗涤剂、制玻璃的原料;(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;(3)CaCO3+2HCl═CaCl2+H2O+CO2↑.
点评 本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
11.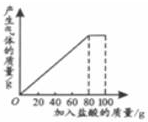 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
(1)第2次加入盐酸后,a为25g.
(2)实验中所用的稀盐酸中,溶质的质量分数是多少?
 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象. | 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(2)实验中所用的稀盐酸中,溶质的质量分数是多少?
12.将同种稀硫酸80g分8次加入10g镁条中(该镁条只含两种物质),测得实验数据见表:
(1)当加入稀硫酸的质量小于20g时没有气体产生,说明的问题是由于镁易于空气中的氧气反应在镁条的表面生成了氧化镁,稀硫酸首先与镁条表面的氧化镁薄膜发生了反应,所以不产生氢气,反应的方程式是:MgO+H2SO4=MgSO4+H2O..
(2)请计算:①10g该镁条中含镁的质量;②若加入20g稀硫酸后立即开始产生气体,求实验所用稀硫酸中溶质的质量分数.
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | 第7次 | 第8次 | |
| 稀硫酸的质量/g | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 生成气体的质量/g | 0 | 0 | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.5 |
(2)请计算:①10g该镁条中含镁的质量;②若加入20g稀硫酸后立即开始产生气体,求实验所用稀硫酸中溶质的质量分数.
14.下列造成空气污染的因素主要由物理变化引起的是( )
| A. | 生活垃圾焚烧产生的有害气体 | B. | 建筑施工导致尘土飞扬 | ||
| C. | 生物腐烂放出的一氧化碳 | D. | 煤燃烧产生的刺激性气味气体 |
15.下列各组中,物质的俗称、学名与化学式表示同一物质的是( )
| A. | 酒精 乙醇 C2H5OH | B. | 纯碱 氢氧化钠 NaOH | ||
| C. | 熟石灰 氧化钙 Ca0 | D. | 干冰 水 H20 |