题目内容
20.关于CO 的叙述不正确的是( )| A. | CO 有可燃性和还原性 | |
| B. | CO 可用排水集气法收集 | |
| C. | CO 有毒,能跟血红蛋白结合,使人体缺氧 | |
| D. | CO 可用向上排空气法收集 |
分析 根据一氧化碳的化学性质(可燃性、还原性、毒性)、物理性质进行分析判断.
解答 解:A、一氧化碳的化学性质比较活泼,具有可燃性、还原性、毒性,故选项说法正确.
B、一氧化碳难溶于水,可用排水集气法收集,故选项说法正确.
C、一氧化碳有毒,极易于血红蛋白结合,使血红蛋白失去于氧结合的能力,使人体缺氧而死,故选项说法正确;
D、一氧化碳的密度和空气相差不大且有毒,不用排空气法收集,故选项说法错误.
故选D.
点评 本题难度不大,掌握一氧化碳的化学性质、物理性质即可正确解答本题.

练习册系列答案
相关题目
11.鉴别CO和H2的最好方法是( )
| A. | 闻气体的气味 | B. | 点燃观察火焰的颜色 | ||
| C. | 点燃后检验其生成物 | D. | 溶解于水 |
15.如表是某城市某日空气质量报告:
某研究性学习小组对表中首要污染物S02:导致酸雨的成因进行探究.
(提示:S02:是一种无色、有刺激性气味的有毒气体,易溶于水,具有与C02相似的化学性质)
【探究实验】实验一:用如图1所示装置进行实验.
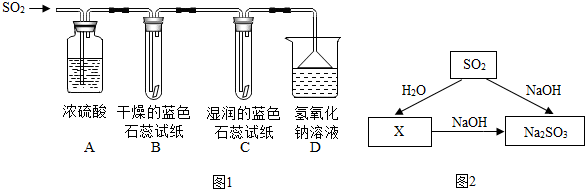
(1)A装置的作用是干燥 SO2气体.
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变红色,说明SO2与水反应生成一种酸.
(3)D装置的作用是吸收SO2,防止污染空气,发生反应的化学方程式是SO2+2NaOH═Na2SO3+H2O.
实验二:往盛有水的烧杯中通人SO2气体,测所得溶液的pH< 7(填“>”“=”或“<”),然后每隔l小时测定其pH,发现pH逐渐变小,直至恒定,说明烧杯中溶液被空气中的氧气氧化最终生成H2SO4.
【查阅资料】SO2形成酸雨的另一途径:S02与空气中的02在飘尘的作用下反应生成SO3
(飘尘的质量和性质在反应前后不发生变化),SO3溶于降水生成H2SO4.在此过程中飘尘作催化剂.
【探究结论】SO2与空气中的氧气、水反应生成硫酸而形成酸雨.该市可能易出现酸雨.
【模拟实验】(1)由于食醋和酸雨的酸度(pH)差不多,
因此酸雨对大理石的作用可以通过大理石碎片放在醋中来模拟.当把2.0g大理石碎片放在醋中一整夜后,取出固体干燥称重,其质量可能是(醋酸钙易溶于水)A.
A.小于2.0gB.正好2.0g C.大于2.0g
(2)这组学生还做了另一个实验,即将大理石碎片放在蒸馏水中过夜,
其实验的目的是作对照,证明对大理石起腐蚀作用的是醋酸而不是水
【知识联想】SO2具有与CO2相似的化学性质,
根据图2给出的SO2及其化合物问的相互转化关系回答:
X的化学式是H2SO3,
写出X与NaOH反应的化学方程H2SO3+2NaOH═Na2SO3+2H2O.
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | S02 | Ⅱ | 良 |
(提示:S02:是一种无色、有刺激性气味的有毒气体,易溶于水,具有与C02相似的化学性质)
【探究实验】实验一:用如图1所示装置进行实验.

(1)A装置的作用是干燥 SO2气体.
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变红色,说明SO2与水反应生成一种酸.
(3)D装置的作用是吸收SO2,防止污染空气,发生反应的化学方程式是SO2+2NaOH═Na2SO3+H2O.
实验二:往盛有水的烧杯中通人SO2气体,测所得溶液的pH< 7(填“>”“=”或“<”),然后每隔l小时测定其pH,发现pH逐渐变小,直至恒定,说明烧杯中溶液被空气中的氧气氧化最终生成H2SO4.
【查阅资料】SO2形成酸雨的另一途径:S02与空气中的02在飘尘的作用下反应生成SO3
(飘尘的质量和性质在反应前后不发生变化),SO3溶于降水生成H2SO4.在此过程中飘尘作催化剂.
【探究结论】SO2与空气中的氧气、水反应生成硫酸而形成酸雨.该市可能易出现酸雨.
【模拟实验】(1)由于食醋和酸雨的酸度(pH)差不多,
因此酸雨对大理石的作用可以通过大理石碎片放在醋中来模拟.当把2.0g大理石碎片放在醋中一整夜后,取出固体干燥称重,其质量可能是(醋酸钙易溶于水)A.
A.小于2.0gB.正好2.0g C.大于2.0g
(2)这组学生还做了另一个实验,即将大理石碎片放在蒸馏水中过夜,
其实验的目的是作对照,证明对大理石起腐蚀作用的是醋酸而不是水
【知识联想】SO2具有与CO2相似的化学性质,
根据图2给出的SO2及其化合物问的相互转化关系回答:
X的化学式是H2SO3,
写出X与NaOH反应的化学方程H2SO3+2NaOH═Na2SO3+2H2O.
5.氧气是与人类关系最密切的一种气体.下列与氧气有关的说法正确的是( )
| A. | 做铁丝在氧气中燃烧实验时,在集气瓶底加少量水来保护集气瓶 | |
| B. | N在纯氧中燃烧生成CO2与H2O,说明N中含有C、H、0三种元素 | |
| C. | 将木炭放在盛有氧气的集气瓶中,木炭就会剧烈燃烧 | |
| D. | 水在通电条件下分解,负极产生氧气 |
12.下列叙述中正确的是( )
| A. | 二氧化碳分子是由一个碳原子和一个氧分子构成的 | |
| B. | 分子一定比原子大 | |
| C. | 不同元素的原子的核电荷数一定不同 | |
| D. | 核外电子排布相同的粒子一定属于同一种元素 |
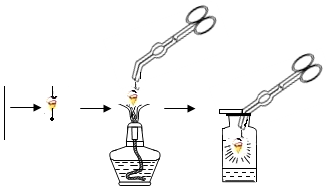 如图是铁丝在在氧气中燃烧的实验,请回答下列问题:
如图是铁丝在在氧气中燃烧的实验,请回答下列问题: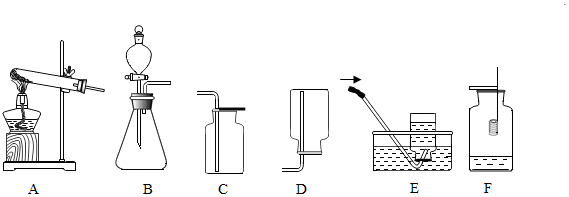
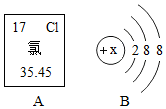 如图中A是氯元素在元素周期表中的相关信息,B是氯离子的结构示意图,分析图中提供的信息,回答问题
如图中A是氯元素在元素周期表中的相关信息,B是氯离子的结构示意图,分析图中提供的信息,回答问题