题目内容
3.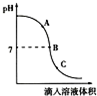 实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示的曲线.
实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示的曲线.(1)在图象中的B点(填“A”“B”或“C”),氢氧化钠和盐酸恰好完全反应.
(2)根据曲线判断,该反应是将盐酸(填“氢氧化钠溶液”或“盐酸”,下同)滴入氢氧化钠溶液中,理由是随着滴入溶液体积的增加,pH减小,最后小于7.
(3)A点时溶液中的溶质为NaOH、NaCl(填化学式),若在此溶液中滴入酚酞试液,溶液显红色.
分析 根据氢氧化钠溶液呈碱性,其pH大于7,盐酸呈酸性,其pH小于7,氢氧化钠溶液和盐酸可以发生中和反应,恰好完全反应时其pH等于7,氢氧化钠过量时显碱性,盐酸过量时显酸性进行分析.
解答 解:(1)通过分析图象可知,B点对应的pH等于7,表明氢氧化钠溶液和稀盐酸恰好完全反应;
(2)根据图象可以看出,开始时溶液的pH大于7,溶液呈碱性,且PH逐渐减小,所以是向氢氧化钠溶液中加入稀盐酸;
(3)从图象可以看出,A点溶液呈碱性,说明溶液中还有没有反应的氢氧化钠,以及反应生成的氯化钠,若在此溶液中滴入酚酞试液,溶液显红色.
故答案为:(1)B;
(2)盐酸,氢氧化钠溶液,随着滴入溶液体积的增加,pH减小,最后小于7;
(3)NaOH、NaCl,红.
点评 本题以图象的形式考查了酸碱中和反应过程中溶液pH的变化,完成此题,要抓住曲线变化的趋势和关键点的意义.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.CO与CO2在性质上不同的原因是( )
| A. | CO难溶于水 | B. | 分子结构不同 | C. | 制法不同 | D. | CO2密度比空气大 |
8.甲、乙、丙、丁四种物质混合后,在一定条件下充分反应,测得反应前后各物质的质量如下表所示,下列判断正确的是( )
| 甲 | 乙 | 丙 | 丁 | |
| 反应前质量/g | 70 | 16 | 8 | 9.5 |
| 反应后质量/g | 38 | 8 | 48 | 9.5 |
| A. | 甲可能是单质,丙一定是化合物 | B. | 乙、丙变化的质量比是1:6 | ||
| C. | 该反应可能是分解反应 | D. | 丁一定是这个反应的催化剂 |
12.下列物质久置于空气中会发生变化,其变化原因与空气成分无直接关系的是( )
| A. | 铝箔 | B. | 浓氨水 | C. | 澄清石灰水 | D. | 铁钉 |
13.下列除杂质的方法不正确的是( )
| 选项 | 物质(括号内为杂质) | 除杂方法 |
| A | N2 (O2) | 通过灼热的铜网 |
| B | CaO (CaCO3) | 高温煅烧 |
| C | CaCl2溶液 (盐酸) | 加入适量的Na2CO3 |
| D | FeCl2溶液(CuCl2) | 加过量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |