题目内容
8.甲、乙、丙、丁四种物质混合后,在一定条件下充分反应,测得反应前后各物质的质量如下表所示,下列判断正确的是( )| 甲 | 乙 | 丙 | 丁 | |
| 反应前质量/g | 70 | 16 | 8 | 9.5 |
| 反应后质量/g | 38 | 8 | 48 | 9.5 |
| A. | 甲可能是单质,丙一定是化合物 | B. | 乙、丙变化的质量比是1:6 | ||
| C. | 该反应可能是分解反应 | D. | 丁一定是这个反应的催化剂 |
分析 根据质量守恒定律和表格中的数据可知,反应后甲质量减少70g-38g=32g,是反应物;反应后乙质量减少16g-8g=8g,是反应物;反应后丙质量增加48g-8g=40g,是生成物;反应前后丁质量不变,可能是催化剂,也可能既不是催化剂,也不是反应物和生成物;因为甲与乙反应生成丙,符合“多变一”的特点,为化合反应.
解答 解:根据质量守恒定律和表格中的数据可知,反应后甲质量减少70g-38g=32g,是反应物;反应后乙质量减少16g-8g=8g,是反应物;反应后丙质量增加48g-8g=40g,是生成物;反应前后丁质量不变,可能是催化剂,也可能既不是催化剂,也不是反应物和生成物;因为甲与乙反应生成丙,符合“多变一”的特点,为化合反应.
A、根据分析,甲与乙反应生成丙,则甲可能是单质,丙一定是化合物,该选项说法正确;
B、乙、丙变化的质量比是(16g-8g):(48g-8g)=1:5,该选项说法不正确;
C、因为甲与乙反应生成丙,符合“多变一”的特点,为化合反应,该选项说法不正确;
D、反应前后丁质量不变,可能是催化剂,也可能既不是催化剂,也不是反应物和生成物,该选项说法不正确.
故选:A.
点评 学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
相关题目
18.下列仪器不能直接在酒精灯上加热的是( )
| A. | 烧杯 | B. | 试管 | C. | 蒸发皿 | D. | 圆底烧瓶 |
16.20℃时,在三个各盛有100g水的容器中分别加入甲、乙、丙三种纯净物(不含结晶水,不与水反应)各10g,充分溶解后,情况如下表所示,有关说法不正确的是( )
| 物 质 | 甲 | 乙 | 丙 |
| 未溶解固体的质量/g | 7 | 0 | 3 |
| A. | 升高温度,三溶液中溶质的质量分数一定会改变 | |
| B. | 三溶液中溶质的质量分数乙>丙>甲 | |
| C. | 所得溶液可能都是饱和溶液 | |
| D. | 20℃时,甲的溶解能力最小 |
20.研究性学习小组对碳酸钠和碳酸氢钠的性质进行探究,请你参与实验.
某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
【查阅资料】
[实验探究]
实验一:探究两者水溶液酸碱性的差异
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变红色,但食用纯碱溶液中颜色更深,由此推测可能食用纯碱溶液碱性更强.小欢认为要比较两种溶液的碱性强弱,可直接用pH试纸进行测定.
实验二:比较两种物质的热稳定性
设计如图(1)装置:小试管套装在带有支管的大试管中,整套装置气密性好,其他装置略去.
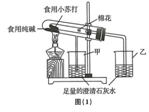 (1)为确保安全,实验结束时,在撤离酒精灯前必须完成的操作是把A、B试管中的导管移出液面.
(1)为确保安全,实验结束时,在撤离酒精灯前必须完成的操作是把A、B试管中的导管移出液面.
(2)现象与结论:装有碳酸氢钠的试管口生成较多的无色小液滴,同时烧杯乙中有大量的气泡产生,澄清石灰水变浑浊;烧杯甲中也有气泡产生,澄清石灰水没有明显变化;实验结束后,经检验大、小两试管内的物质均是碳酸钠.结合以上实验,可得出结论:①碳酸氢钠受热生成的物质是碳酸钠、水和二氧化碳.②在受热条件下,碳酸钠比碳酸氢钠稳定.
实验三:比较与盐酸反应生成相同体积二氧化碳气体的快慢
取碳酸氢钠4.2g放入如图Ⅰ装置的锥形瓶中,取碳酸钠5.3g放入另一相同装置的锥形瓶中,分别加入相同质量、相同浓度的盐酸(足量).相同的条件下,通过图Ⅱ装置测量出生成气体的体积,得到时间-体积关系曲线如图Ⅲ所示.
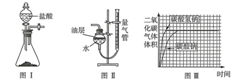
(4)已知二氧化碳不溶于该油层,图Ⅱ装置中油层的作用是防止部分的二氧化碳溶于水,造成实验误差.
(5)数据与分析:根据图Ⅲ曲线,可得出有关“比较与盐酸反应生成相同体积二氧化碳气体的快慢”的结论是在相同的条件下生成相同体积的二氧化碳,碳酸氢钠与盐酸反应比碳酸钠与盐酸反应快.
(6)反思与讨论:实验中“取碳酸氢钠4.2g、碳酸钠5.3g”的目的是生成相同体积的二氧化碳.
某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
【查阅资料】
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液呈碱性 | 水溶液呈碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
实验一:探究两者水溶液酸碱性的差异
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变红色,但食用纯碱溶液中颜色更深,由此推测可能食用纯碱溶液碱性更强.小欢认为要比较两种溶液的碱性强弱,可直接用pH试纸进行测定.
实验二:比较两种物质的热稳定性
设计如图(1)装置:小试管套装在带有支管的大试管中,整套装置气密性好,其他装置略去.
 (1)为确保安全,实验结束时,在撤离酒精灯前必须完成的操作是把A、B试管中的导管移出液面.
(1)为确保安全,实验结束时,在撤离酒精灯前必须完成的操作是把A、B试管中的导管移出液面.(2)现象与结论:装有碳酸氢钠的试管口生成较多的无色小液滴,同时烧杯乙中有大量的气泡产生,澄清石灰水变浑浊;烧杯甲中也有气泡产生,澄清石灰水没有明显变化;实验结束后,经检验大、小两试管内的物质均是碳酸钠.结合以上实验,可得出结论:①碳酸氢钠受热生成的物质是碳酸钠、水和二氧化碳.②在受热条件下,碳酸钠比碳酸氢钠稳定.
实验三:比较与盐酸反应生成相同体积二氧化碳气体的快慢
取碳酸氢钠4.2g放入如图Ⅰ装置的锥形瓶中,取碳酸钠5.3g放入另一相同装置的锥形瓶中,分别加入相同质量、相同浓度的盐酸(足量).相同的条件下,通过图Ⅱ装置测量出生成气体的体积,得到时间-体积关系曲线如图Ⅲ所示.

(4)已知二氧化碳不溶于该油层,图Ⅱ装置中油层的作用是防止部分的二氧化碳溶于水,造成实验误差.
(5)数据与分析:根据图Ⅲ曲线,可得出有关“比较与盐酸反应生成相同体积二氧化碳气体的快慢”的结论是在相同的条件下生成相同体积的二氧化碳,碳酸氢钠与盐酸反应比碳酸钠与盐酸反应快.
(6)反思与讨论:实验中“取碳酸氢钠4.2g、碳酸钠5.3g”的目的是生成相同体积的二氧化碳.
 a、b、c三物质的溶解度曲线如图所示,请回答下列问题:
a、b、c三物质的溶解度曲线如图所示,请回答下列问题: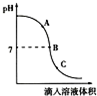 实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示的曲线.
实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示的曲线. 写出下列有关铁的现象及方程式
写出下列有关铁的现象及方程式