题目内容
9.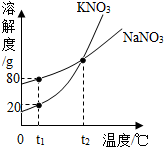 如图表示是KNO3和NaNO3的溶解度曲线.下列说法正确的是( )
如图表示是KNO3和NaNO3的溶解度曲线.下列说法正确的是( )| A. | t1℃时,两种溶液中溶质质量分数一定不相等 | |
| B. | t1℃时,在50g水里加入15g KNO3固体,充分溶解,得到60g溶液 | |
| C. | t1℃时,硝酸钾、硝酸钠两物质饱和溶液升温到t2℃后,溶质质量分数相等 | |
| D. | 两种饱和溶液从t2℃降温到t1℃时,析出晶体:硝酸钾一定多于硝酸钠 |
分析 A、据该温度下两种物质的溶解度大小分析解答;
B、据该温度下硝酸钾的溶解度分析所加物质是否能全部溶解;
C、硝酸钾、硝酸钠的溶解度均随温度升高而增大,并结合升温前两物质的溶解度分析解答;
D、等质量的饱和溶液降低相同的温度,溶解度变化大的析出晶体多.
解答 解:A、由图可知:硝酸钾的溶解度小于硝酸钠的溶解度,若将小于或等于20g的溶质放于100g水中,则两溶液中溶质均能全部溶解,溶质的质量分数相等,故错误;
B、t1℃时硝酸钾的溶解度是20g,即100g水中最多溶解20g的硝酸钾,所以在50g水里加入15g KNO3固体,最多溶解10g,不能全部溶解,得到60g溶液,正确;
C、t1℃时硝酸钾的溶解度小于硝酸钠的溶解度,饱和时质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%,即溶解度大则溶质的质量分数大,则硝酸钾的溶质质量分数小于硝酸钠的质量分数;硝酸钾、硝酸钠两物质饱和溶液升温到t2℃后,溶液中溶质、溶剂的质量不变,溶质的质量分数与升温前相等,所以硝酸钠的溶解度大于硝酸钾溶质质量分数,故错误;
D、不知两种饱和溶液的质量,无法确定两种饱和溶液从t2℃降温到t1℃时,析出晶体的质量多少,若两溶液相等,则析出晶体质量相等,故错误;
故选:B.
点评 本题难度不大,主要考查了溶解度概念、饱和溶液中溶解度大则溶质质量分数大、固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力.

练习册系列答案
相关题目
20.分析、类比和推理是化学学习中常用的思维方法.下列分析、类比和推理正确的是( )
| A. | 酸雨的pH小于7,所以pH小于7的雨水一定是酸雨 | |
| B. | 酸中都含有氢元素,所以含有氢元素的化合物一定是酸 | |
| C. | 中和反应有盐和水生成,所以有盐和水生成的反应一定是中和反应 | |
| D. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 |
17. 中国最新战机歼-31使用了高强度、耐高温的钛合金材料.工业上冶炼钛的反应如下:TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2.下列有关该反应的说法正确的是( )
中国最新战机歼-31使用了高强度、耐高温的钛合金材料.工业上冶炼钛的反应如下:TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2.下列有关该反应的说法正确的是( )
 中国最新战机歼-31使用了高强度、耐高温的钛合金材料.工业上冶炼钛的反应如下:TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2.下列有关该反应的说法正确的是( )
中国最新战机歼-31使用了高强度、耐高温的钛合金材料.工业上冶炼钛的反应如下:TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2.下列有关该反应的说法正确的是( )| A. | 化合反应 | B. | 复分解反应 | C. | 分解反应 | D. | 置换反应 |
4.2015年诺贝尔医学奖授予第一个证实青蒿素可以在动物体和人体内有效抵抗疟疾的中国科学家屠呦呦.关于青蒿素(C15H22O5)的下列说法正确的是( )
| A. | 青蒿素由碳、氢、氧三个元素组成 | |
| B. | 青蒿素中碳、氧元素的质量比为3:1 | |
| C. | 青蒿素由碳原子、氢原子和氧原子构成 | |
| D. | 青蒿素中氢元素的质量分数最小 |
14.分类是学习和研究化学的常用方法.下列分类中正确的是( )
| A. | 有机物:甲烷、酒精、甲醛 | |
| B. | 复合肥料:尿素、硝酸钾、磷酸氢二铵 | |
| C. | 混合物:煤、石油、冰水共存物 | |
| D. | 合成材料:合金、合成橡胶、合成纤维 |
18.以下变化中,氢元素由游离态变为化合态的是( )
| A. | 氢气液化 | B. | 电解水 | C. | 双氧水分解 | D. | 氢气燃烧 |
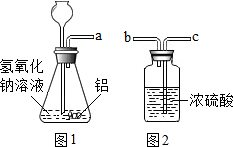
 铝是目前人们在生产、生活中使用较多的一种金属.
铝是目前人们在生产、生活中使用较多的一种金属.