题目内容
4.2015年诺贝尔医学奖授予第一个证实青蒿素可以在动物体和人体内有效抵抗疟疾的中国科学家屠呦呦.关于青蒿素(C15H22O5)的下列说法正确的是( )| A. | 青蒿素由碳、氢、氧三个元素组成 | |
| B. | 青蒿素中碳、氧元素的质量比为3:1 | |
| C. | 青蒿素由碳原子、氢原子和氧原子构成 | |
| D. | 青蒿素中氢元素的质量分数最小 |
分析 A.根据元素的规定来分析;
B.根据化合物中元素的质量比来分析;
C.根据物质的结构来分析;
D.根据化合物中元素的质量比来分析.
解答 解:A.元素是个宏观概念,只讲种类、不讲个数,故错误;
B.青蒿素中碳、氧元素的质量比为(12×15):(16×5)=9:4,故错误;
C.青蒿素是由青蒿素分子构成的,而不是由原子直接构成的,故错误;
D.青蒿素中碳、氢、氧三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40,可见其中氢元素的质量分数最小,故正确.
故选D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
15.物质的变化就在我们身边.如图所示的变化属于物理变化的是( )
| A. |  豆腐切块 | B. |  光合作用 | C. |  烧制茶杯 | D. |  蚕豆制酱 |
19.下列关于金属的说法正确的是( )
| A. | 波尔多液的配制可以在铁制容器中进行 | |
| B. | 铝制品抗腐蚀能力较铁制品强 | |
| C. | 用ZnCl2溶液、Fe和Cu三种物质能验证Zn、Fe、Cu三种金属的活动性强弱顺序 | |
| D. | 生活中不用金属银而用铜或铝做导线的原因是银的导电性比铜、铝差 |
9.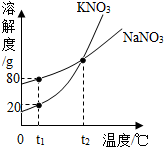 如图表示是KNO3和NaNO3的溶解度曲线.下列说法正确的是( )
如图表示是KNO3和NaNO3的溶解度曲线.下列说法正确的是( )
 如图表示是KNO3和NaNO3的溶解度曲线.下列说法正确的是( )
如图表示是KNO3和NaNO3的溶解度曲线.下列说法正确的是( )| A. | t1℃时,两种溶液中溶质质量分数一定不相等 | |
| B. | t1℃时,在50g水里加入15g KNO3固体,充分溶解,得到60g溶液 | |
| C. | t1℃时,硝酸钾、硝酸钠两物质饱和溶液升温到t2℃后,溶质质量分数相等 | |
| D. | 两种饱和溶液从t2℃降温到t1℃时,析出晶体:硝酸钾一定多于硝酸钠 |
16.下列说法中错误的是( )
| A. | 溶液都是由一种溶质和一种溶剂组成的 | |
| B. | 溶液里各部分的性质是相同的 | |
| C. | 只要条件不变,糖水里的糖不会分离出来 | |
| D. | 通常不指明溶剂的溶液是水溶液 |
10.哪一组硫元素的化合价为+6价( )
| A. | SO2和SO3 | B. | H2S和SO3 | C. | H2S和H2S03 | D. | Na2SO4和SO3 |

