题目内容
1.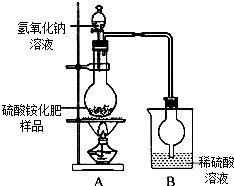 硫酸铵是常用的一种氮肥,现有一种硫酸铵化肥,为测定其中硫酸铵的质量分数,采用如图(甲)所示的装置进行实验.已知在A、B中所发生反应的化学方程式如下:(NH4)2SO4+2NaOH$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+Na2SO4 2NH3+H2SO4═(NH4)2SO4(注:反应生成的NH3能被烧杯中的稀硫酸溶液完全吸收)
硫酸铵是常用的一种氮肥,现有一种硫酸铵化肥,为测定其中硫酸铵的质量分数,采用如图(甲)所示的装置进行实验.已知在A、B中所发生反应的化学方程式如下:(NH4)2SO4+2NaOH$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+Na2SO4 2NH3+H2SO4═(NH4)2SO4(注:反应生成的NH3能被烧杯中的稀硫酸溶液完全吸收)(1)实验过程中,需往烧瓶中加入足量浓氢氧化钠溶液并充分加热的原因是使硫酸铵完全反应.
(2)方案评价根据右图实验设计测得的数据,计算出硫酸铵的质量分数可能偏高,因为实验装置的设计存在一个明显缺陷A、B装置之间缺少一个干燥装置.
(3)现称取27g硫酸铵化肥样品,用改进后的实验装置重新进行实验,实验后测得B装置的质量增加了6.8g.
请通过计算确定该化肥中硫酸铵的质量分数.(计算结果准确到0.1%)
分析 ①根据加入足量的氢氧化钠溶液能使硫酸铵完全反应解答;
②B增重是吸收氨气的质量,如果水进入B,则计算的数据偏大,据此解答;
②B增重的质量为生成氨气的质量,根据它算出硫酸铵的质量,再进一步求出样品中硫酸铵的质量;
解答 解:(1)往烧瓶中加入足量浓氢氧化钠溶液并充分加热可以使硫酸铵完全反应,故填:使硫酸铵完全反应;
(2)B吸收的氨气,由于有水进入,故会导致加过偏大,因此需要在AB之间加一个干燥装置,故填:A、B装置之间缺少一个干燥装置;
(3)增重的6.8g为氨气的质,设27g样品中含有(NH4)2SO4的质量为x:
(NH4)2SO4+2NaOH$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4+2NH3↑+2H2O
132 34
x 6.8g
$\frac{132}{x}=\frac{34}{6.8g}$
x=26.4g
该化肥中硫酸铵的质量分数=$\frac{26.4g}{27g}$×100%≈97.8%
答:化肥中硫酸铵的质量分数为97.8%.
点评 本题主要考查了实验室制取氨气的实验,掌握反应原理是解答的关键,题目较综合.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
9.实验室现要配制溶质的质量分数为10%的氯化钠溶液50克,下列实验操作会使称量或测量得到的数值偏小的是( )
| A. | 用砝码已生锈的天平称量固体药品 | |
| B. | 用湿润的pH试纸测量稀盐酸的pH | |
| C. | 称量时砝码已等于药品质量、游码未归零 | |
| D. | 用量筒量取45ml液体时,俯视读数,实际量取液体的体积 |
6.下列实验操作正确的是( )
| A. |  称量固体 | B. |  加入大理石 | C. |  读液体体积 | D. |  过滤河水 |
13.化学式为 NH3、NH4Cl 和(NH4)2SO4 的三种化合物中氮元素的百分含量,从大到小的排列顺序是( )
| A. | (NH4)2SO4,NH4Cl,NH3 | B. | NH3,(NH4)2SO4,NH4Cl | ||
| C. | NH3,NH4Cl,(NH4)2SO4 | D. | NH4Cl,(NH4)2SO4,NH3 |
10.聪聪同学在实验室帮老师整理废弃药品时发现一瓶没有标签的绿色粉末,对其组成很好奇.征得老师允许后,设计了如表实验进行探究.将表格填写完整.
为了进一步确定该物质的元素组成,查阅部分资料后,他继续进行了实验.
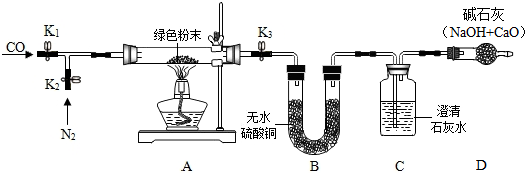
【实验步骤】
①如图搭建实验仪器,并检验装置的气密性.
②在A装置中装入11.1g绿色粉末.关闭K1,打开K2、K3,持续通入适量N2.
③关闭K2、K3,分别称量装置B、C、D的质量,记录数据.
④打开K3,点燃酒精灯加热绿色粉末直至装置C中无气泡产生时,关闭K3,熄灭酒精灯.分别称量装置B、C、D的质量,记录数据.
⑤待A冷却后,打开K1、K3,持续通入适量CO,再次点燃酒精灯加热
⑥当A中粉末全部变红后,熄灭酒精灯.试管冷却后,关闭K1.称量装置A、B、C、D的质量.
【实验现象和数据处理】
【实验分析与反思】
老师看了实验方案后认为,从环保的角度来看,此装置有一个缺陷,建议装置D后还应添加一个酒精灯,并在实验步骤⑤(填实验步骤的序号)中点燃.
(2)步骤②通入氮气的目的是将试管内的空气排尽,避免空气中的水蒸气和二氧化碳影响实验
【实验结论】
该绿色粉末的化学式为Cu2(OH)2CO3.
| 操作步骤 | 实验现象 | 结论或化学反应方程式 |
| 取少量样品于试管中,加入足量稀硫酸,将试管用导管与澄清石灰水相连. | ①产生大量气体,使澄清石灰水变浑浊. ②样品全部溶解,溶液呈蓝色. | ①样品中含有CO32-离子 ②样品中含有Cu2+离子 |
| 在上述蓝色溶液中,插入一根洁净的铁丝. | ①铁丝表面产生少量气泡. ②同时铁丝表面出现红色物质. | 写出②中的反应方程式Fe+CuSO4=Cu+FeSO4 |

【实验步骤】
①如图搭建实验仪器,并检验装置的气密性.
②在A装置中装入11.1g绿色粉末.关闭K1,打开K2、K3,持续通入适量N2.
③关闭K2、K3,分别称量装置B、C、D的质量,记录数据.
④打开K3,点燃酒精灯加热绿色粉末直至装置C中无气泡产生时,关闭K3,熄灭酒精灯.分别称量装置B、C、D的质量,记录数据.
⑤待A冷却后,打开K1、K3,持续通入适量CO,再次点燃酒精灯加热
⑥当A中粉末全部变红后,熄灭酒精灯.试管冷却后,关闭K1.称量装置A、B、C、D的质量.
【实验现象和数据处理】
| 装置A | 装置B | 装置C | 装置D | |
| 第一次 加热后 | 绿色粉末变为黑色 | 白色粉末变蓝色 质量增加0.9g | 出现白色沉淀, 质量增加2.2g | 无明显变化 质量不改变 |
| 第二次 加热后 | 黑色粉末变红色 质量为6.4g | 无明显变化, 质量不改变 | 沉淀先增加后部分溶解; 质量增加 | 无明显变化 质量不改变 |
老师看了实验方案后认为,从环保的角度来看,此装置有一个缺陷,建议装置D后还应添加一个酒精灯,并在实验步骤⑤(填实验步骤的序号)中点燃.
(2)步骤②通入氮气的目的是将试管内的空气排尽,避免空气中的水蒸气和二氧化碳影响实验
【实验结论】
该绿色粉末的化学式为Cu2(OH)2CO3.


