题目内容
13.化学式为 NH3、NH4Cl 和(NH4)2SO4 的三种化合物中氮元素的百分含量,从大到小的排列顺序是( )| A. | (NH4)2SO4,NH4Cl,NH3 | B. | NH3,(NH4)2SO4,NH4Cl | ||
| C. | NH3,NH4Cl,(NH4)2SO4 | D. | NH4Cl,(NH4)2SO4,NH3 |
分析 分别根据元素质量分数的计算方法求出这三种物质中含碳元素的质量分数,比较大小即可.(注:也可以在分子相同的情况下比较分母的大小得到质量分数的大小关系).
解答 解:①NH3的相对分子质量是14+3=17,
②氯化铵NH4Cl的相对分子质量是14+4+35.5=53.5,
③硫酸铵(NH4)2SO4的相对分子质量是(14+4)×2+32+64=132
含氮的质量分数分别是
①$\frac{14}{17}$×100%=82.4%,
②$\frac{14}{53.5}$×100%≈26.2%,
③$\frac{28}{132}$×100%≈21.2%,
所以按含氮的质量分数从大到小顺序排列为①>②>③.
故选C
点评 主要考查了相对分子质量,元素质量分数的计算.
某元素的质量分数=$\frac{该元素分子的相对原子质量×原子个数}{相对分子质量}$×100%.
化学式中各原子的相对原子质量的总和,就是相对分子质量.

练习册系列答案
相关题目
3.某科学小组的同学利用混有少量H2O、CO2的CO气体还原氧化铜,并验证反应后的气体产物.实验室现有如图所示实验装置(可重复使用).按气体从左到右的方向,装置连接顺序正确的是( )
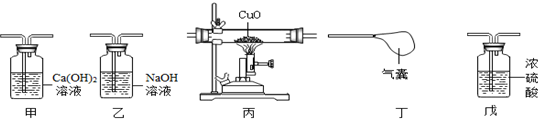

| A. | 甲→乙→丙→丁→戊 | B. | 甲→丙→乙→戊→丁 | ||
| C. | 乙→甲→戊→丙→甲→丁 | D. | 乙→甲→丙→戊→乙→丁 |
4.要除去下列各组物质中的少量杂质,所选试剂和方法不可行的是( )
| 选项 | 物质 | 杂质 | 试剂、方法 |
| A | O2 | 水蒸气 | 通过浓H2SO4洗气 |
| B | MnO2 | 炭粉 | 在空气中灼烧 |
| C | KCl溶液 | BaCl2 | 加入适量的Na2SO4溶液,过滤 |
| D | FeSO4溶液 | CuSO4 | 加入足量铁屑,充分反应后过滤 |
8.化学研究物质的性质和用途,请体会并填写下表:
| 物质用途 | 金刚石切割玻璃 | 石墨作电极 | 活性炭净水 | 氧气用于炼钢 | 干冰用于人工降雨 | 氮气保护食品 |
| 对应特性 | ①硬度最大 | ②良好的导电性 | ③吸附性 | ④氧化性 | ⑤易升华 | ⑥性质稳定 |
18.在下列变化中,既属于化合反应,又属于氧化反应的是( )
| A. | 用高锰酸锰制氧气 | B. | 硫粉在氧气中燃烧 | ||
| C. | 用氯酸钾和二氧化锰制氧气 | D. | 石蜡在空气中燃烧 |
3.下列化学反应属于分解反应的是( )
| A. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | B. | CO2+H2O═H2CO3 | ||
| C. | 2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O | D. | Ca(HCO3)2═CaCO3↓+CO2↑+H2O |
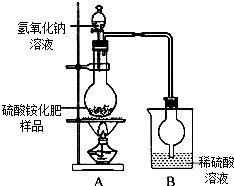 硫酸铵是常用的一种氮肥,现有一种硫酸铵化肥,为测定其中硫酸铵的质量分数,采用如图(甲)所示的装置进行实验.已知在A、B中所发生反应的化学方程式如下:(NH4)2SO4+2NaOH$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+Na2SO4 2NH3+H2SO4═(NH4)2SO4(注:反应生成的NH3能被烧杯中的稀硫酸溶液完全吸收)
硫酸铵是常用的一种氮肥,现有一种硫酸铵化肥,为测定其中硫酸铵的质量分数,采用如图(甲)所示的装置进行实验.已知在A、B中所发生反应的化学方程式如下:(NH4)2SO4+2NaOH$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+Na2SO4 2NH3+H2SO4═(NH4)2SO4(注:反应生成的NH3能被烧杯中的稀硫酸溶液完全吸收)