题目内容
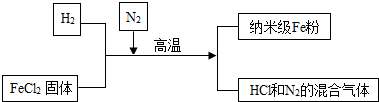
13.初中化学中的几种常见物质由如图所示的转化关系(部分反应物和生成物已略去),其中反应②常用于工业生产,反应③常用于实验室制备F气体.请回答下列问题:
(1)D的化学式是CaCO3;A的化学式可能是Na2CO3(任写一种);
(2)反应③的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)F气体的用途灭火、气体肥料;(写两种)
(4)在四种基本反应类型中,上图未涉及的反应类型是置换反应.
分析 根据图中D属于沉淀且高温煅烧生成F气体和E固体,E固体还能与水反应生成G溶液,G溶液与F气体反应还能生成D,结合反应②常用于工业生产,即碳酸钙高温生成氧化钙和二氧化碳,因此D可以是碳酸钙,E是氧化钙,F是二氧化碳,氧化钙与水反应生成氢氧化钙,G是氢氧化钙,氢氧化钙与二氧化碳生成碳酸钙和水,又因为反应③常用于实验室制备F-二氧化碳气体,实验室制取二氧化碳是碳酸钙与盐酸反应,生成氯化钙、水、二氧化碳,所以B溶液是氯化钙溶液,由A溶液与氯化钙反应生成碳酸钙沉淀和C溶液,所以A溶液是碳酸盐,可以是碳酸钠或碳酸钾等物质;据此完成相关的问题.
解答 解:根据图中D属于沉淀且高温煅烧生成F气体和E固体,E固体还能与水反应生成G溶液,G溶液与F气体反应还能生成D,结合反应②常用于工业生产,即碳酸钙高温生成氧化钙和二氧化碳,因此D可以是碳酸钙,E是氧化钙,F是二氧化碳,氧化钙与水反应生成氢氧化钙,G是氢氧化钙,氢氧化钙与二氧化碳生成碳酸钙和水,又因为反应③常用于实验室制备F-二氧化碳气体,实验室制取二氧化碳是碳酸钙与盐酸反应,生成氯化钙、水、二氧化碳,所以B溶液是氯化钙溶液,由A溶液与氯化钙反应生成碳酸钙沉淀和C溶液,所以A溶液是碳酸盐,可以是碳酸钠或碳酸钾等物质;代入检验,符合题意.
(1)根据分析,D是碳酸钙,A可能为碳酸钠等碳酸盐,故D的化学式是CaCO3;A的化学式可能是Na2CO3(或K2CO3等)(任写一种);
(2)根据反应③常用于实验室制备F-二氧化碳气体,故反应③的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)根据分析,F是二氧化碳,F气体的用途灭火、气体肥料等;
(4)从上述化学反应中反应①③是复分解反应,反应②分解反应;反应④是化合反应,反应⑤不属于基本反应类型.故在四种基本反应类型中,上图未涉及的反应类型是置换反应.
故答案为:
(1)CaCO3; Na2CO3;
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)灭火、气体肥料;(4)置换反应.
点评 本题属于常见物质的框图式推断题,解答本题关键是要知道实验室制取二氧化碳的方法,熟悉碳酸钙高温生成氧化钙、二氧化碳,氧化钙与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应生成碳酸钙和水.


| A. | 分子在化学变化中不可再分 | |
| B. | 化学反应前后原子的种类和数目都不变 | |
| C. | 该反应是既不是化合反应也不是分解反应 | |
| D. | 反应后生成了两种新的化合物 |
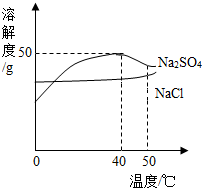 如图是硫酸钠和氯化钠的溶解度曲线,下列说法正确的是( )
如图是硫酸钠和氯化钠的溶解度曲线,下列说法正确的是( )| A. | 温度升高两种物质的溶解度都增大 | |
| B. | 50℃的Na2SO4饱和溶液降到40℃时有晶体析出 | |
| C. | 40℃时,Na2SO4的饱和溶液中溶质与溶剂的质量比为1:2 | |
| D. | 可用降温结晶的方法提纯含少量Na2SO4的NaCl |
【提出问题】氢氧化钠溶液是否变质?
【查阅资料】氯化钠溶液、氯化钡溶液呈中性.
【实验探究】小王、小李两同学分别设计了不同方案并加以实验.
| 实验步骤 | 实验现象 | 结论 | |
| 小王 | 用pH试纸测溶液的pH | 溶液的pH>7 | 说明氢氧化钠溶液没有变质 |
| 小李 | 取少量溶液于试管中,加入适量氯化钡溶液 | A | 说明氢氧化钠溶液已经变质 |
(2)小李同学的实验中观察到实验现象A为白色沉淀产生.该反应的化学方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl.
(3)小张同学认为该氢氧化钠溶液只是部分变质.为确定小张同学的猜想,应该对小李同学的实验进行如下改进:向试管中加入过量的氯化钡溶液,再向试管中滴加酚酞试液,通过观察溶液颜色变化来检验该溶液是否含有氢氧化钠.
(4)小王同学在测定溶液pH实验中,由于紧张先将pH试纸润湿后再去测氢氧化钠溶液的pH,你认为他测出该溶液的pH会偏小(填“偏大”、“偏小”或“不变”).
【反思】
(5)该氢氧化钠溶液变质的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示).
【拓展应用】
(6)要证明氢氧化钠溶液是否变质,你认为还可使用与小李实验所加试剂不同类别的试剂是HCl(填一种试剂即可,用化学式填写).

 如图是关于氧气的制取与性质实验装置图.回答下列问题:
如图是关于氧气的制取与性质实验装置图.回答下列问题: