题目内容
2.某校化学兴趣小组同学在实验室整理药品时,发现氢氧化钠溶液的试剂瓶未塞瓶塞,且试剂瓶口周围有一些白色固体,他们怀疑氢氧化钠已经变质,于是进行了如下实验探究.【提出问题】氢氧化钠溶液是否变质?
【查阅资料】氯化钠溶液、氯化钡溶液呈中性.
【实验探究】小王、小李两同学分别设计了不同方案并加以实验.
| 实验步骤 | 实验现象 | 结论 | |
| 小王 | 用pH试纸测溶液的pH | 溶液的pH>7 | 说明氢氧化钠溶液没有变质 |
| 小李 | 取少量溶液于试管中,加入适量氯化钡溶液 | A | 说明氢氧化钠溶液已经变质 |
(2)小李同学的实验中观察到实验现象A为白色沉淀产生.该反应的化学方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl.
(3)小张同学认为该氢氧化钠溶液只是部分变质.为确定小张同学的猜想,应该对小李同学的实验进行如下改进:向试管中加入过量的氯化钡溶液,再向试管中滴加酚酞试液,通过观察溶液颜色变化来检验该溶液是否含有氢氧化钠.
(4)小王同学在测定溶液pH实验中,由于紧张先将pH试纸润湿后再去测氢氧化钠溶液的pH,你认为他测出该溶液的pH会偏小(填“偏大”、“偏小”或“不变”).
【反思】
(5)该氢氧化钠溶液变质的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示).
【拓展应用】
(6)要证明氢氧化钠溶液是否变质,你认为还可使用与小李实验所加试剂不同类别的试剂是HCl(填一种试剂即可,用化学式填写).
分析 氢氧化钠能与二氧化碳反应生成碳酸钠和水,检验变质就是检验碳酸钠的存在,检验变质的程度就是检验氢氧化钠是否存在,据此解答.
解答 解:(1)碳酸钠溶液呈碱性,能使酚酞试液变红,故填:碳酸钠溶液也能使酚酞溶液变红;
(2)碳酸钠能与氯化钡反应生成碳酸钡沉淀和氯化钠,故填:白色沉淀产生,BaCl2+Na2CO3=BaCO3↓+2NaCl;
(3)要检验变质的程度,就是检验氢氧化钠的存在,需要加入过量的氯化钡除去碳酸钠,故填:过量;
(4)先将pH试纸润湿后再去测氢氧化钠溶液的pH,则他测出该溶液的pH会偏小,故填:偏小;
(5)氢氧化钠变质是氢氧化钠与二氧化碳反应生成了碳酸钠和水,故填:2NaOH+CO2═Na2CO3+H2O;
(6)要检验氢氧化钠变质,还可以加入盐酸,观察产生气泡,故填:HCl.
点评 本题考查的是物质变质成分的实验探究的知识,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
12.某校化学兴趣小组同学在实验室整理药品时,发现氢氧化钠溶液的试剂瓶未塞瓶塞,且试剂瓶口周围有一些白色固体,他们怀疑氢氧化钠已经变质,于是进行了如下实验探究.
【提出问题】氢氧化钠溶液是否变质?
【查阅资料】氯化钠溶液、氯化钡溶液呈中性.
【实验探究】小王、小李两同学分别设计了不同方案并加以实验.
(1)小李同学认为小王同学的结论不科学,其理由是Na2CO3溶液也显碱性,即使NaOH变质,溶液的pH也大于7.
(2)小李同学的实验中观察到实验现象A为产生白色沉淀,该反应的化学方程式为Na2CO3+BaCl2=2NaCl+BaCO3↓.
【拓展应用】
(3)若要除去上述变质的氢氧化钠溶液中的杂质应加入适量的Ba(OH)2(填化学式)溶液而除去.
【提出问题】氢氧化钠溶液是否变质?
【查阅资料】氯化钠溶液、氯化钡溶液呈中性.
【实验探究】小王、小李两同学分别设计了不同方案并加以实验.
| 实验步骤 | 实验现象 | 结论 | |
| 小王 | 用pH试纸测溶液的pH | 溶液的pH>7 | 说明氢氧化钠溶液没有变质 |
| 小李 | 取少量溶液于试管中,加入适量氯化钡溶液 | A | 说明氢氧化钠溶液已经变质 |
(2)小李同学的实验中观察到实验现象A为产生白色沉淀,该反应的化学方程式为Na2CO3+BaCl2=2NaCl+BaCO3↓.
【拓展应用】
(3)若要除去上述变质的氢氧化钠溶液中的杂质应加入适量的Ba(OH)2(填化学式)溶液而除去.
17.下列实验方法不能达到实验目的是( )
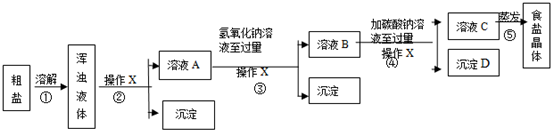
| A. | 除去粗盐中的难溶性杂质--将粗盐溶解、过滤、蒸发 | |
| B. | 除去CO中的CO2---通入足量的氢氧化钠溶液 | |
| C. | 除去热水瓶胆中的水垢--用食醋 | |
| D. | 鉴别稀盐酸、氢氧化钠溶液、氯化钠溶液--滴加无色酚酞溶液 |
7.下列化学用语与含义相符的是( )
| A. | 3O--3个氧原子 | B. | CO2--1个二氧化碳分子 | ||
| C. | O2--2个氧原子 | D. | $\stackrel{+3}{Fe}$--带3个单位正电荷的铁离子 |
14.废弃的易拉罐和塑料瓶属于( )
| A. | 厨余垃圾 | B. | 可回收垃圾 | C. | 不可回收垃圾 | D. | 有害垃圾 |

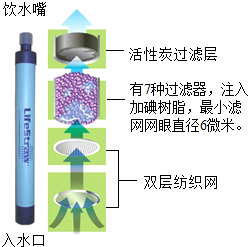 电视节目《荒野求生》中的生命吸管(如图所示)是一种将污水净化为饮用水的吸管装置,可以除去99.3% 的细菌和病毒,但难以除去汞等金属离子.回答下列问题:
电视节目《荒野求生》中的生命吸管(如图所示)是一种将污水净化为饮用水的吸管装置,可以除去99.3% 的细菌和病毒,但难以除去汞等金属离子.回答下列问题: