题目内容
5.硝酸铵是重要的氮肥.计算:(1)硝酸铵中各元素的质量比N:H:O=7:1:12.
(2)某块农田要施加35千克氮元素,需要硝酸铵的质量是80千克.
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)硝酸铵中氮、氢、氧元素的质量之比是(14×2):(1×4):(16×3)=7:1:12.故填:N:H:O=7:1:12;
(2)设需要硝酸铵的质量为x,则x×$\frac{14×2}{14×2+1×4+16×3}×100%$=35kg
x=80kg
故答案为:80.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
15.下列实验现象或实验原理正确的是( )
| A. | 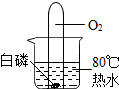 白磷始终不燃烧 | B. | 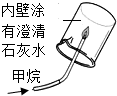 验证甲烷燃烧生成二氧化碳和水 | ||
| C. | 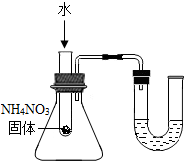 U形管内液面左高右低 | D. | 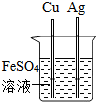 验证Fe、Cu、Ag的金属或定性强弱 |
17.下列实验方法不能达到实验目的是( )
| A. | 除去粗盐中的难溶性杂质--将粗盐溶解、过滤、蒸发 | |
| B. | 除去CO中的CO2---通入足量的氢氧化钠溶液 | |
| C. | 除去热水瓶胆中的水垢--用食醋 | |
| D. | 鉴别稀盐酸、氢氧化钠溶液、氯化钠溶液--滴加无色酚酞溶液 |
14.废弃的易拉罐和塑料瓶属于( )
| A. | 厨余垃圾 | B. | 可回收垃圾 | C. | 不可回收垃圾 | D. | 有害垃圾 |
15.物质P和物质Q在一定条件下可以相互转化(均是一步反应),下列选项不符合题意的是( )
| A. | P是O2 Q是CO2 | B. | P是NaCl Q是NaNO3 | ||
| C. | P是Fe Q是Fe3O4 | D. | P是CO2 Q是CaCO3 |
