题目内容
1.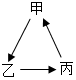 甲、乙、丙分别是不同类别的物质,且均含的相同元素为地壳中含量最高的元素,且甲可做食品干燥剂.它们之间转化关系如图所示(部分物质和反应条件已略去).
甲、乙、丙分别是不同类别的物质,且均含的相同元素为地壳中含量最高的元素,且甲可做食品干燥剂.它们之间转化关系如图所示(部分物质和反应条件已略去).(1)乙与一种盐反应转化为丙的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,如图转化关系中一定不会涉及到的基本反应类型是置换反应.
(2)若甲中混有少量丙,除去丙时发生反应的化学方程式为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
分析 根据题干提供的信息进行分析解答,甲、乙、丙三种物质三种物质均含地壳中含量最多的元素.则都含有氧元素,甲能做食品干燥剂,因此甲是生石灰,则丙是碳酸钙;氧化钙能够转化为乙,则乙是熟石灰.据此解答.
解答 解:甲、乙、丙三种物质三种物质均含地壳中含量最多的元素.则都含有氧元素,甲能做食品干燥剂,因此甲是生石灰,则丙是碳酸钙;氧化钙能够转化为乙,则乙是熟石灰,带入框图,推断合理;因此:
(1)氢氧化钙和碳酸钠反应可以产生碳酸钙沉淀和氢氧化钠,该反应属于复分解反应,碳酸钙分解产生氧化钙和二氧化碳,属于分解反应;氧化钙和水反应产生氢氧化钙,属于化合反应,因此没有置换反应;故填:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;置换反应;
(2)氧化钙混有碳酸钙,可以通过高温煅烧的方法除去碳酸钙,故填:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
点评 本题是框图式物质推断题,解答本题的关键是找准解题的突破口,直接得出有关物质的化学式,然后顺推或逆推得出其他物质的化学式.

练习册系列答案
相关题目
12.根据下表信息,相关说法正确的是( )
| 温度/℃ | 溶解度/g | |||
| NaCl | Kcl | NH4Cl | KNO3 | |
| 20 | 36.0 | 34.0 | 37.2 | 31.6 |
| 40 | 36.6 | 40.0 | 45.8 | 63.9 |
| 60 | 37.3 | 45.5 | 55.2 | 110 |
| A. | 20℃时,NaCl的溶液度为36.0 | |
| B. | 40℃时,KCl饱和溶液的溶质质量分数为40% | |
| C. | 40℃时,向100g水中加入50gNH4Cl充分溶解,溶液质量为145.8g | |
| D. | 60℃时降温到20℃时,KNO3和KCl的饱和溶液析出晶体较多的是KNO3 |
13.下列实验方案设计不合理的是( )
| 实验目的 | 实验方案 | |
| A | 除去二氧化碳中的一氧化碳 | 将气体通入氢氧化钠溶液 |
| B | 检验甲烷中是否含有氢元素 | 点燃,在火焰上方罩一干冷的烧杯,观察现象 |
| C | 区别棉线和羊毛线 | 分别灼烧,闻气味 |
| D | 除去食盐中的泥沙 | 溶解、过滤、蒸发 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
16.有铁粉和铜粉的均匀混合物,三位同学分别取该混合物等溶质质量分数的稀硫酸反应,分别得出甲、乙、丙三组数据,如表所示:
请利用已学的知识和分析数据,回答下列问题:
(1)写出发生反应的化学方程式:Fe+H2SO4═FeSO4+H2↑
该反应的现象为
①固体部分溶解,产生气泡
②溶液由无色变成浅绿色
③反应容器底部有残留固体
(2)分析甲、乙两组数据可知10g金属混合物中铜的质量为4g.再分析甲、丙两组数据可知,甲同学所得溶液中含有溶质的是FeSO4(填化学式)
(3)丙组所得溶液中溶质的质量分数为15.4%.(计算结果精确到0.1%)
| 甲 | 乙 | 丙 | |
| 取用金属混合物的质量 | 10 | 10 | 20 |
| 取用稀硫酸的质量/g | 100 | 200 | 100 |
| 反应后过滤,得干燥固体的质量/g | 4 | 4 | 14 |
(1)写出发生反应的化学方程式:Fe+H2SO4═FeSO4+H2↑
该反应的现象为
①固体部分溶解,产生气泡
②溶液由无色变成浅绿色
③反应容器底部有残留固体
(2)分析甲、乙两组数据可知10g金属混合物中铜的质量为4g.再分析甲、丙两组数据可知,甲同学所得溶液中含有溶质的是FeSO4(填化学式)
(3)丙组所得溶液中溶质的质量分数为15.4%.(计算结果精确到0.1%)
6.实验室中有一瓶含有少量氯化钠和不可溶性杂质的硫酸钠样品.某化学兴趣小组对该样品成分进行定量测定,甲、乙、丙三位同学分别称取一定质量的样品放入烧杯中,溶入足量水后过滤得到滤液;再向滤液中加入一定质量的氯化钡溶液,充分反应后过滤,将沉淀洗涤、干燥并称量.相关实验数据记录如下:
请回答下列问题:
计算该样品中硫酸钠的质量分数.(写出计算步骤,计算结果保留到0.1%)
| 称量项目 | 甲 | 乙 | 丙 |
| 所取样品的质量/g | 15 | 15 | 20 |
| 加入氯化钡溶液的质量/g | 150 | 100 | 100 |
| 反应后所得沉淀的质量/g | 23.3 | 23.3 | 23.3 |
计算该样品中硫酸钠的质量分数.(写出计算步骤,计算结果保留到0.1%)
11.下列图示实验操作中,正确的是( )
| A. | 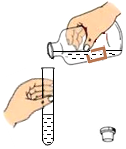 | B. |  | C. | 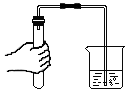 | D. |  |

