题目内容
7.按酸、碱、盐、氧化物的顺序排列的一组物质是( )| A. | H2SO4 NH3•H2O Na2CO3 CO2 | |
| B. | HCl CaO NaHCO3 CO | |
| C. | SO3 Ba(OH)2 NaCl H2O2 | |
| D. | HNO3 C2H5OH NH4Cl H2O |
分析 根据物质的类别进行分析判断即可,酸是指电离时产生的阳离子全部是氢离子的化合物;碱是指电离时产生的阴离子全部是氢氧根离子的化合物;盐是由金属阳离子和酸根阴离子构成的物质;氧化物是由两种元素组成且其中一种是氧元素的化合物,据此解答.
解答 解:A、H2SO4属于酸,NH3•H2O属于碱,Na2CO3属于盐,CO2属于氧化物,故A正确;
B、HCl属于酸,CaO属于氧化物,NaHCO3属于盐,CO属于氧化物,故B错误;
C、SO3属于氧化物,Ba(OH)2属于碱,NaCl属于盐,H2O2属于氧化物,故C错误;
D、HNO3属于酸,C2H5OH属于有机物,不属于碱,NH4Cl属于盐,H2O属于氧化物,故D错误;
故选A.
点评 本题考查了常见物质的分类,完成此题,可以依据有关的概念结合物质的组成进行.

练习册系列答案
相关题目
17.如图是氨气和氧气在点燃条件下,发生化学反应时部分微观示意图.下列说法正确的是( )
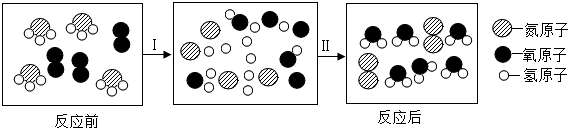

| A. | 反应中各元素的化合价均发生变化 | B. | 该反应属于置换反应 | ||
| C. | 生成物中两种物质的质量比为3:1 | D. | 该反应中分子、原子都发生了改变 |
2.乙酸乙酯( C4H8O2)常用作食品、饮料的调香剂.下列有关乙酸乙酯的叙述正确的是( )
| A. | 由14个原子构成 | |
| B. | 其中碳元素的质量分数为41.4% | |
| C. | 一个乙酸乙酯分子中,碳、氢、氧原子的个数比为2:4:1 | |
| D. | 其中碳、氢、氧元素的质量比为12:1:16 |
19.华在自家厨房中发现一袋未开封的白色粉末状食用物,包装袋上的字迹不太清楚,于是他带到化学实验室和小组同学一起探究其成分.
【提出问题】包装袋内的白色粉末到底是什么物质?
【猜想假设】猜想1:可能是食盐;
猜想2:可能是淀粉;
猜想3:可能是纯碱(化学式为Na2CO3);
猜想4:可能是小苏打.
【资料查阅】(1)有关物质的信息如下:
(2)碳酸氢钠受热易分解生成碳酸钠和二氧化碳等,碳酸钠受热不分解.
【实验探究】
(1)小彤取样品放入适量的水中,搅拌形成了无色溶液,于是她排除了猜想2.
(2)小青取上述少量溶液,向其中滴加酚酞试液,溶液变红,他推断出该白色粉末一定不是猜想1.小华由此现象认为猜想3正确,但小组成员都认为小华的结论不严密,理由是小苏打溶液也显碱性,也能使酚酞试液变红.
【交流提升】
小组成员认为可以通过加热或定量实验来确定粉末的组成.于是该小组又进行了下面的实验:
【反思拓展】
小苏打也可用作治疗胃酸过多的药剂,反应的原理为NaHCO3+HCl=NaCl+H2O+CO2↑(用化学方程式表示).
【提出问题】包装袋内的白色粉末到底是什么物质?
【猜想假设】猜想1:可能是食盐;
猜想2:可能是淀粉;
猜想3:可能是纯碱(化学式为Na2CO3);
猜想4:可能是小苏打.
【资料查阅】(1)有关物质的信息如下:
| 物质 | 氯化钠 | 纯碱 | 小苏打 |
| 常温下的溶解度/g | 36 | 21.5 | 9.6 |
| 常温下的稀溶液的pH | 7 | 11 | 9 |
【实验探究】
(1)小彤取样品放入适量的水中,搅拌形成了无色溶液,于是她排除了猜想2.
(2)小青取上述少量溶液,向其中滴加酚酞试液,溶液变红,他推断出该白色粉末一定不是猜想1.小华由此现象认为猜想3正确,但小组成员都认为小华的结论不严密,理由是小苏打溶液也显碱性,也能使酚酞试液变红.
【交流提升】
小组成员认为可以通过加热或定量实验来确定粉末的组成.于是该小组又进行了下面的实验:
| 方案 | 实验操作 | 实验现象 | 实验结论 |
| 1.加热法 | 取一定量的样品于试管中,加热,将产生的气体通入澄清的石灰水 | 澄清的石灰水变浑浊 | 猜想4正确 |
| 2.定量法 | 取15g样品,加入100mL常温下的水,搅拌 | 有固体剩余 |
小苏打也可用作治疗胃酸过多的药剂,反应的原理为NaHCO3+HCl=NaCl+H2O+CO2↑(用化学方程式表示).
16.CaO和NaOH固体的混合物,俗名“碱石灰”,实验室常用作干燥剂,碱石灰在空气久置会吸收空气中的水和二氧化碳而变质,某实验小组为确定一瓶久置的碱石灰样品的成分,设计下列实验流程.请你参与探究过程:
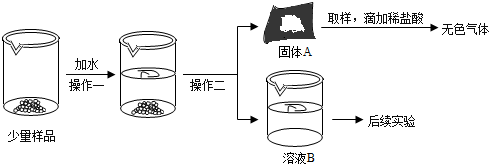
(1)为了使样品充分溶解,操作一定还要用到的玻璃仪器是玻璃棒;操作二的名称是过滤.
(2)固体A中一定含有碳酸钙(填名称).
(3)溶液B成分的探究.
[查阅资料]
①Ca(OH)2、Na2CO3溶于水无明显的温度变化;
②Na2CO3溶液呈碱性,能使酚酞试液变红;
[提出猜想]
溶液B中溶质可能为:①NaOH; ②Na2CO3; ③NaOH和Na2CO3;④Ca(OH)2和NaOH(填化学式)
[设计方案并进行实验]
甲、乙同学分别设计如下方案并进行探究:
甲同学:取少量溶液B于试管中,滴加足量的稀盐酸,产生大量气泡,则溶液B中的溶质是Na2CO3.
乙同学:取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,则溶液B中的溶质一定含有NaOH.
[反思与评价]
丙同学认真分析上述二位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断.他认为B溶液中一定含有Na2CO3,可能含有NaOH.为进一步确认溶液B中是否含NaOH,做做了如下实验.
实验步骤①的目的是除尽溶液B中的Na2CO3,避免干扰NaOH的检验.
(4)实验过程中,同学们发现向样品中加水时还放出大量的热.综合以上探究,下列对样品成分分析正确的是BD(填序号).
A.一定有NaOH B.一定有Na2CO3 C.一定有CaO D.至少有NaOH、CaO中的一种.

(1)为了使样品充分溶解,操作一定还要用到的玻璃仪器是玻璃棒;操作二的名称是过滤.
(2)固体A中一定含有碳酸钙(填名称).
(3)溶液B成分的探究.
[查阅资料]
①Ca(OH)2、Na2CO3溶于水无明显的温度变化;
②Na2CO3溶液呈碱性,能使酚酞试液变红;
[提出猜想]
溶液B中溶质可能为:①NaOH; ②Na2CO3; ③NaOH和Na2CO3;④Ca(OH)2和NaOH(填化学式)
[设计方案并进行实验]
甲、乙同学分别设计如下方案并进行探究:
甲同学:取少量溶液B于试管中,滴加足量的稀盐酸,产生大量气泡,则溶液B中的溶质是Na2CO3.
乙同学:取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,则溶液B中的溶质一定含有NaOH.
[反思与评价]
丙同学认真分析上述二位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断.他认为B溶液中一定含有Na2CO3,可能含有NaOH.为进一步确认溶液B中是否含NaOH,做做了如下实验.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,在滤液中滴加酚酞试液 | ①有白色沉淀生成 ②溶液由无色变为红色 | 猜想③正确 |
(4)实验过程中,同学们发现向样品中加水时还放出大量的热.综合以上探究,下列对样品成分分析正确的是BD(填序号).
A.一定有NaOH B.一定有Na2CO3 C.一定有CaO D.至少有NaOH、CaO中的一种.
 2016年8月5日-21日,第31届夏季奥林匹克运动会将在巴西的里约热内卢举行.根据里约奥运会官网的描述,里约奥运会火炬由再生铝和树脂材料制造而成.上面绘有5条不同色彩的曲线,分别代表大地、海洋、山脉、天空和太阳,同时还对应着巴西国旗的颜色.
2016年8月5日-21日,第31届夏季奥林匹克运动会将在巴西的里约热内卢举行.根据里约奥运会官网的描述,里约奥运会火炬由再生铝和树脂材料制造而成.上面绘有5条不同色彩的曲线,分别代表大地、海洋、山脉、天空和太阳,同时还对应着巴西国旗的颜色.