题目内容
16.CaO和NaOH固体的混合物,俗名“碱石灰”,实验室常用作干燥剂,碱石灰在空气久置会吸收空气中的水和二氧化碳而变质,某实验小组为确定一瓶久置的碱石灰样品的成分,设计下列实验流程.请你参与探究过程: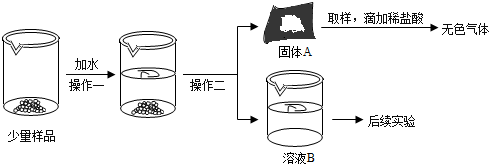
(1)为了使样品充分溶解,操作一定还要用到的玻璃仪器是玻璃棒;操作二的名称是过滤.
(2)固体A中一定含有碳酸钙(填名称).
(3)溶液B成分的探究.
[查阅资料]
①Ca(OH)2、Na2CO3溶于水无明显的温度变化;
②Na2CO3溶液呈碱性,能使酚酞试液变红;
[提出猜想]
溶液B中溶质可能为:①NaOH; ②Na2CO3; ③NaOH和Na2CO3;④Ca(OH)2和NaOH(填化学式)
[设计方案并进行实验]
甲、乙同学分别设计如下方案并进行探究:
甲同学:取少量溶液B于试管中,滴加足量的稀盐酸,产生大量气泡,则溶液B中的溶质是Na2CO3.
乙同学:取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,则溶液B中的溶质一定含有NaOH.
[反思与评价]
丙同学认真分析上述二位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断.他认为B溶液中一定含有Na2CO3,可能含有NaOH.为进一步确认溶液B中是否含NaOH,做做了如下实验.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,在滤液中滴加酚酞试液 | ①有白色沉淀生成 ②溶液由无色变为红色 | 猜想③正确 |
(4)实验过程中,同学们发现向样品中加水时还放出大量的热.综合以上探究,下列对样品成分分析正确的是BD(填序号).
A.一定有NaOH B.一定有Na2CO3 C.一定有CaO D.至少有NaOH、CaO中的一种.
分析 (1)根据溶解所需的仪器以及过滤的原理进行解答;
(2)根据碳酸钙不溶于水以及能和稀盐酸反应放出二氧化碳气体进行解答;
(3)[猜想]:根据氧化钙和氢氧化钠的性质进行解答;根据氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,加入足量CaCl2溶液这样会除掉全部的碳酸钠;
(4)根据氧化钙或者是氢氧化钠固体溶于水时放热进行解答.
解答 解:(1)为了使样品充分溶解,操作一定还要用到的玻璃仪器是玻璃棒;过滤的原理是分离溶于水的固体和不溶于水的固体,所以操作二的名称是过滤;
(2)碳酸钙不溶于水以及能和稀盐酸反应放出二氧化碳气体,固体A中一定含有:碳酸钙;
(3)[提出猜想]因为氧化钙和水反应生成氢氧化钙;所以溶液B中溶质可能为:①NaOH; ②Na2CO3; ③NaOH和Na2CO3;④Ca(OH)2和NaOH;
[反思与评价]:现象为白色沉淀生成、溶液由无色变为红色;
氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,CaCl2+Na2CO3=2NaCl+CaCO3↓,加入足量CaCl2溶液这样会除掉全部的碳酸钠,避免干扰NaOH的检验;
(4)氧化钙或者是氢氧化钠固体溶于水时放热,综合以上探究,下列对样品成分分析正确的是一定有Na2CO3,至少有NaOH、CaO中的一种.
故答案为:
(1)玻璃棒;过滤;(2)碳酸钙(CaCO3);(3)NaOH;白色沉淀生成、溶液由无色变为红色;
除尽溶液B中的Na2CO3,避免干扰NaOH的检验;(4)BD.
点评 熟练掌握碳酸钠、碳酸钙等碳酸盐和氢氧化钠、氧化钙的化学性质,能根据所给的实验或者自己设计实验来验证它们是否变质,并熟练的写出相应的化学方程式.

练习册系列答案
相关题目
7.按酸、碱、盐、氧化物的顺序排列的一组物质是( )
| A. | H2SO4 NH3•H2O Na2CO3 CO2 | |
| B. | HCl CaO NaHCO3 CO | |
| C. | SO3 Ba(OH)2 NaCl H2O2 | |
| D. | HNO3 C2H5OH NH4Cl H2O |
4.下列说法错误的是( )
| A. | 过量施用化肥和农药可造成水污染 | |
| B. | 回收利用废旧金属,可节约金属资源 | |
| C. | 开发和利用太阳能、风能符合“低碳生活” | |
| D. | 汽车燃料燃烧产生的CO2,是造成酸雨的主要原因 |
11.明确宏观现象的微观本质是学习化学的重要思想,下列说选正确的是( )
| A. | 水通电分解生成氢气和氧气,是因为水中含有氢分子和氧分子 | |
| B. | 水结成冰,是因为温度降低,分子停止运动 | |
| C. | 水与冰的共存物是纯净物,是因为它们由同种分子构成 | |
| D. | 水与酒精混合液的体积小于混合前二者体积之和,是因为混合后分子体积变小 |
3.最新表明,药物丁西他滨(分子式:C28H20O10N5P)对急性髓性白血病和骨髓增生异常综合征患者具有生物和临床效果,并且患者的耐受性良好.下列有关丁西他滨说法正确的是( )
| A. | 每一个丁西他滨分子是由64个原子构成 | |
| B. | 丁西他滨分子是由五种元素组成 | |
| C. | 丁西他滨中磷元素质量分数最小 | |
| D. | 丁西他滨中氢元素与氧元素质量比是13:5 |
10.下列实验方案不可行的是( )
| A. | 用灼烧的方法区别腈纶制品和羊毛制品 | |
| B. | 用酚酞试液区分氢氧化钠溶液和碳酸钠溶液 | |
| C. | 用高温灼烧氧化铁和木炭粉混合物的方法制取少量铁 | |
| D. | 用加水溶解的方法区别NaOH、Na2SO4、NH4NO3三种白色固体 |
8.2.4g某纯净物完全燃烧后生成4.4gCO2和1.8g水.则对该物质相关判断正确的是( )
| A. | 该物质只含碳、氢元素 | |
| B. | 该物质一定含有碳、氢元素,可能含有氧元素 | |
| C. | 该物质一定含碳、氢、氧三种元素 | |
| D. | 该物质分子中碳原子和氢原子的个数比为1:1 |

 一天,小晨去郊游,在路上意外发现了几枚铜钱,上面有经色斑点.这些绿色斑点是怎么形成的?它的主要成分是什么?具有什么性质?围绕这些问题,她与同学们一起进行了如下探究活动:
一天,小晨去郊游,在路上意外发现了几枚铜钱,上面有经色斑点.这些绿色斑点是怎么形成的?它的主要成分是什么?具有什么性质?围绕这些问题,她与同学们一起进行了如下探究活动: