题目内容
14.如表表示KNO3和KCl的溶解度列表,下列说法正确的是( )| 温度/℃ | 20 | 30 | 40 | 50 | |
| 溶解度/g | KNO3 | 31.6 | 45.8 | 63.9 | 85.5 |
| KCl | 34.0 | 37.0 | 40.0 | 42.6 | |
| A. | KNO3的溶解度大于KCl的溶解度 | |
| B. | 在20~30℃之间这两种物质的溶解度可能相等 | |
| C. | 40℃时向100g水中加40gKCl得到40%的溶液 | |
| D. | 50℃时向100g水中加90gKNO3可得到190g溶液 |
分析 A、没有指明温度无法比较溶解度的大小;
B、分析图表,KNO3和KCl的溶解度曲线在20℃~30℃温度范围内相交;
C、依据40℃时KCl的溶解度是40g分析解答;
D、根据50℃时KNO3的溶解度分析解答.
解答 解:A、没有指明温度无法比较溶解度的大小,故A错误;
B、分析图表,KNO3和NaCl的溶解度曲线在20℃~30℃温度范围内有相同的时候,所以两种物质的溶解度曲线在此范围内相交,故B正确;
C、40℃时KCl的溶解度是40g,相当于100g水最多溶解氯化钾40g,质量分数为:$\frac{40g}{100g+40g}×100%$=28.6%,错误;
D、50℃时KNO3的溶解度为85.5g,即100g水最多溶解硝酸钾85.5g,可得到185.5g溶液,错误.
故选B.
点评 在某一温度时,若两种物质的溶解度相等,则它们的饱和溶液中溶质的质量分数相等.若没有指明饱和溶液,则溶质的质量分数就不一定相等.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
9.小红发现自己家的铁锅在与水面接触的部位最易生锈;小兰发现自己的铜制眼镜框表面出现了绿色的铜锈;
小花发现吃剩苹果的果肉上会产生一层暗褐色物质,好象生了“锈”一般.
【提出问题】:这三种物质“生锈”的原因是什么?
【收集证据】:(1)回忆已有知识:铁生锈的条件是与水和氧气接触.
(2)查阅有关资料:“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中的氧气发生了一系列的反应,生成暗褐色的物质.
(3)实验探究:将四小块铜片分别按下图所示放置一个月,观察现象如下,装置Ⅱ中氢氧化钠溶液和碱石灰的作用是吸收二氧化碳;写出装置Ⅱ氢氧化钠溶液中发生反应的化学方程式:CO2+2NaOH=Na2CO3+H2O.
(4)由实验可知:铜生锈是铜与水、氧气、二氧化碳等物质共同作用的结果.
【得出结论】(5)经过交流讨论,三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与氧气有关.
小花发现吃剩苹果的果肉上会产生一层暗褐色物质,好象生了“锈”一般.
【提出问题】:这三种物质“生锈”的原因是什么?
【收集证据】:(1)回忆已有知识:铁生锈的条件是与水和氧气接触.
(2)查阅有关资料:“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中的氧气发生了一系列的反应,生成暗褐色的物质.
(3)实验探究:将四小块铜片分别按下图所示放置一个月,观察现象如下,装置Ⅱ中氢氧化钠溶液和碱石灰的作用是吸收二氧化碳;写出装置Ⅱ氢氧化钠溶液中发生反应的化学方程式:CO2+2NaOH=Na2CO3+H2O.
| 实验 装置 | 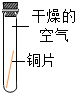 | 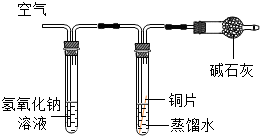 | 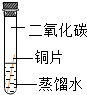 | 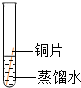 |
| 实验 现象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面 附近锈蚀最严重 |
【得出结论】(5)经过交流讨论,三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与氧气有关.
19.空气是一种宝贵的自然资源,下列气体不可直接从空气分离获得的是( )
| A. | 用作医疗急救的氧气 | B. | 用作焊接保护气的稀有气体 | ||
| C. | 用作清洁燃料的氢气 | D. | 用作食品防腐剂的氮气 |
3.掌握正确的实验操作是进行化学实验的基础,下列实验基本操作错误的是( )
| A. |  蒸发食盐水 | B. |  取用固体 | C. |  称量氯化钠 | D. |  收集氧气 |
 材料的应用,极大地促进了人类社会的发展和人们生活水平的提高.请从化学视角回答下列问题:
材料的应用,极大地促进了人类社会的发展和人们生活水平的提高.请从化学视角回答下列问题: