题目内容
10.现代社会汽车大量增加,发生交通事故的一个重要原因是遇到意外情况时车不能立即停止.(1)白酒、红酒和啤酒中均含有乙醇(俗称酒精),饮酒后酒精可进入人体血液中.请问:乙醇(C2H5OH)中碳、氧、氢元素的质量比是C:O:H=12:8:3.
(2)在治理酒后驾车中,酒精检测仪发挥了重要作用.其中的化学反应原理是将红色的三氧化铬转变为绿色的一种铬盐X,其反应方程式可表示为:C2H5OH+4CrO3+6H2SO4═2X+2CO2↑+9H2O,则X的化学式是Cr2(SO4)3.
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
解答 解:(1)乙醇中碳、氢、氧元素的质量比为(12×2):(16×1):(1×6)=12:8:3.
(2)根据反应的化学方程式C2H5OH+4CrO3+6H2SO4═2X+2CO2↑+9H2O,反应物中碳、氢、氧、铬、硫原子个数分别为2、24、37、4、6,反应后的生成物中碳、氢、氧、铬、硫原子个数分别为2、18、13、0、0,根据反应前后原子种类、数目不变,则2X中含有4个铬原子、6个硫原子和24个O原子,则每个X分子由2个铬原子、3个硫原子和3个氧原子构成,则物质X的化学式为Cr2(SO4)3.
故答案为:(1)12:8:3;(2)Cr2(SO4)3.
点评 本题难度不大,灵活运用化学式的有关计算、利用化学反应前后原子守恒来确定物质的化学式是正确解题的关键.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
15.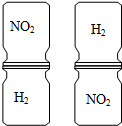 把红棕色的NO2气体和无色的H2的集气瓶,按如图两种方式放置,然后抽去两瓶之间的玻璃片,可观察到左边的两瓶气体的颜色很快趋于一致,右边的两瓶需较长时间才能达到同样的效果,由此现象不能得出的结论是( )
把红棕色的NO2气体和无色的H2的集气瓶,按如图两种方式放置,然后抽去两瓶之间的玻璃片,可观察到左边的两瓶气体的颜色很快趋于一致,右边的两瓶需较长时间才能达到同样的效果,由此现象不能得出的结论是( )
 把红棕色的NO2气体和无色的H2的集气瓶,按如图两种方式放置,然后抽去两瓶之间的玻璃片,可观察到左边的两瓶气体的颜色很快趋于一致,右边的两瓶需较长时间才能达到同样的效果,由此现象不能得出的结论是( )
把红棕色的NO2气体和无色的H2的集气瓶,按如图两种方式放置,然后抽去两瓶之间的玻璃片,可观察到左边的两瓶气体的颜色很快趋于一致,右边的两瓶需较长时间才能达到同样的效果,由此现象不能得出的结论是( )| A. | 分子是在不断运动 | B. | 分子之间有间隔 | ||
| C. | 氢气的密度比二氧化氮小 | D. | 分子由原子构成 |
19.下列有关比较,正确的是( )
| A. | 密度:空气<氧气 | |
| B. | 沸点:液氧<液氮 | |
| C. | 化学活泼性:氧气<氮气 | |
| D. | 二氧化碳的含量:空气>人体呼出的气体 |



