题目内容
18.氢氧化钠.氢氧化钙都属于碱,除这两种碱外,常用的碱还有氢氧化钾,氨水等.分析 根据已有的碱进行分析解答,常见的碱是氢氧化钙、氢氧化钠、氢氧化钾和氨水,据此解答.
解答 解:常见的碱是氢氧化钙、氢氧化钠、氢氧化钾和氨水,故填:氢氧化钾,氨水.
点评 本题考查的是常见的碱的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
8.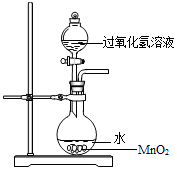 用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:
用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:
猜想1:加水可以起到稀释的作用,使反应速度变缓. 猜想2:…
并根据猜想进行了实验:每次取15毫升15%的过氧化氢溶液,稀释成不同溶质质量分数,在其他条件相同的情况下进行实验.记录数据如下:
(1)实验室用过氧化氢制氧气的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)过氧化氢溶液的溶质质量分数对反应速度有怎样的影响?一定范围内,过氧化氢溶质质量分数越大反应速度越快.
(3)根据表中数据可知,该同学的猜想2是:加水可以给溶液降温.
 用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:
用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:猜想1:加水可以起到稀释的作用,使反应速度变缓. 猜想2:…
并根据猜想进行了实验:每次取15毫升15%的过氧化氢溶液,稀释成不同溶质质量分数,在其他条件相同的情况下进行实验.记录数据如下:
| 实验 | 1 | 2 | 3 | 4 | 5 |
| 过氧化氢溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% |
| MnO2粉末用量/克 | 0.5 | 0.5 | 0.5 | 0.5 | 0.5 |
| 收集到500mL气体时所用时间/秒 | 560 | 186 | 103 | 35 | 12 |
| 反应后液体温度/℃ | 26 | 38 | 43 | 59 | 71 |
(2)过氧化氢溶液的溶质质量分数对反应速度有怎样的影响?一定范围内,过氧化氢溶质质量分数越大反应速度越快.
(3)根据表中数据可知,该同学的猜想2是:加水可以给溶液降温.
9.下列说法中,不正确的是( )
| A. | 物理变化过程中,分子本身发生了变化 | |
| B. | 分子是由原子构成的 | |
| C. | 原子是化学变化中的最小微粒 | |
| D. | 化学反应的实质是原子的重新组合 |
6.下列溶液中溶质都是酸的是( )
| A. | H+、Na+、Cl-、NO3- | B. | H+、SO42-、Cl-、NO3- | ||
| C. | K+、Na+、Cl-、NO3- | D. | Ca2+、SO42-、Cl-、NO3- |
3.某兴趣小组同学用大理石和盐酸反应制取二氧化碳,将制得的气体通入澄清石灰水,观察到石灰水未变浑浊,他们对此现象产生了好奇.同学们提出了下列三个假设:
假设①:石灰水已变质;假设②:制得的气体中无二氧化碳;假设③:制得的气体中有一定量的氯化氢气体.
(1)同学们先探究假设①是否成立.他们将适量的原试剂瓶中的澄清的石灰水倒入小试管中,然后通入二氧化碳气体(填写实验操作),他们根据实验现象确认了石灰水未变质.他们接着探究,通过实验否定了假设②.
(2)同学们继续设计了两个实验来探究假设③,如表所示:
上述实验一中的A物质是硝酸银溶液,实验二中的实验现象是产生气泡
(3)同学们通过实验确定了澄清石灰水未变浑浊的原因是制得的气体中含有一定量的氯化氢气体.请解释将制得的气体通入澄清石灰水后,石灰水不变浑浊的原因是稀盐酸和氢氧化钙反应生成了氯化钙和水.
假设①:石灰水已变质;假设②:制得的气体中无二氧化碳;假设③:制得的气体中有一定量的氯化氢气体.
(1)同学们先探究假设①是否成立.他们将适量的原试剂瓶中的澄清的石灰水倒入小试管中,然后通入二氧化碳气体(填写实验操作),他们根据实验现象确认了石灰水未变质.他们接着探究,通过实验否定了假设②.
(2)同学们继续设计了两个实验来探究假设③,如表所示:
| 实验操作 | 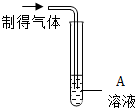 | 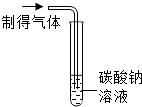 |
| 实验现象 | 出现白色沉淀 | ? |
| 实验结论 | 制得的气体中有氯化氢气体 | 制得的气体中有氯化氢气体 |
(3)同学们通过实验确定了澄清石灰水未变浑浊的原因是制得的气体中含有一定量的氯化氢气体.请解释将制得的气体通入澄清石灰水后,石灰水不变浑浊的原因是稀盐酸和氢氧化钙反应生成了氯化钙和水.
7.某同学在学习了燃烧的有关知识后,了解到木炭在氧气中比在空气中燃烧的更旺;他还联想到古语道:“人要实,火要虚”的含义,做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺.于是引发思考,并进行了实验探究.请你参与其中回答下面有关问题:
【发现问题】可燃物燃烧的剧烈程度与哪些因素有关呢?
【提出猜想】猜想①:燃烧的剧烈程度可能与氧气浓度有关;
猜想②:燃烧的剧烈程度可能与反应物接触面积有关.
【验证猜想】实验报告如下:
【结论应用】请你结合工业生产或生活中的实例,就如何使燃料得到充分燃烧,而达到节约能源的目的,提出一条具体的建议:增大燃料和空气或氧气的接触面积,或增大氧气的浓度.
【发现问题】可燃物燃烧的剧烈程度与哪些因素有关呢?
【提出猜想】猜想①:燃烧的剧烈程度可能与氧气浓度有关;
猜想②:燃烧的剧烈程度可能与反应物接触面积有关.
【验证猜想】实验报告如下:
| 验证猜想 | 对比实验操作 | 实验现象 | 实验结论 |
| 猜想① | 将蜡烛分别在空气和纯氧中点燃 | 蜡烛在 氧气中燃烧 比在空气中燃烧更剧烈 | 氧气浓度 越大 燃烧越剧烈 |
| 猜想② | 将质量相同的木炭块 和木炭粉分别放在 氧气中燃烧 | 木炭粉比木炭块 燃烧 更剧烈 | 接触面积 越大 燃烧越剧烈 |
8.能证明分子在化学反应中可以再分的变化是( )
| A. | 碘受热变成碘蒸气 | B. | 一定条件下二氧化碳制干冰 | ||
| C. | 铁块研磨成铁粉 | D. | 氧化汞受热放出氧气 |