题目内容
5.在工业上用纯碱和石灰石为原料制备烧碱,主要流程如图所示: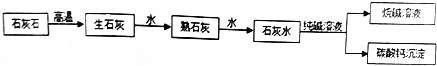
(1)检验烧碱溶液中含有少量Na2CO3的具体方法是取适量溶液于试管中,滴加适量的氯化钙溶液,产生白色沉淀,说明氢氧化钠溶液中含有碳酸钠.
(2)在室温下,将53g质量分数为10%的Na2CO3溶液与3000g澄清石灰水充分混合,恰好完全反应.则这时所得NaOH溶液的质量是多少?
分析 碳酸钠能和氯化钙反应生成白色沉淀碳酸钙和氯化钠;
碳酸钠和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)检验烧碱溶液中含有少量Na2CO3的具体方法是:取适量溶液于试管中,滴加适量的氯化钙溶液,产生白色沉淀,说明氢氧化钠溶液中含有碳酸钠.
故填:取适量溶液于试管中,滴加适量的氯化钙溶液,产生白色沉淀,说明氢氧化钠溶液中含有碳酸钠.
(2)解:设生成碳酸钙质量为x,
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,
106 100
53g×10% x
$\frac{106}{53g×10%}$=$\frac{100}{x}$,
x=5g,
这时所得NaOH溶液的质量是:53g+3000g-5g=3048g,
答:这时所得NaOH溶液的质量是3048g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
15.下列物质混合后,仍然是纯净物的是( )
| A. | 氧气和臭氧 | B. | 冰和干冰 | C. | 铅笔芯和铅 | D. | 酒精和乙醇 |
16.下列实验现象的描述说法正确的是( )
| A. | 打开盛有浓盐酸的瓶盖,看到瓶口有白烟产生 | |
| B. | 在铜绿中加入稀硫酸,溶液变为蓝色 | |
| C. | 在装有干燥的氨气的集气瓶中,放入干燥的红色石蕊试纸,试纸变蓝 | |
| D. | 在久置于空气中的生石灰中加盐酸有气泡产生 |
13.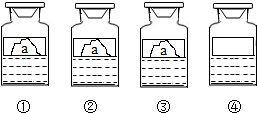 实验室由于操作或保存药品不当,标签常常易损毁.现有四瓶溶液①②③④由于操作不当标签已经破损(如图),但是已经知道这四瓶溶液分别是NaOH、Ca(OH)2、Na2CO3、KCl溶液中的一种,某兴趣小组同学决定对四瓶标签破损溶液成分进行探究(只提供稀盐酸和酚酞溶液两种药品):
实验室由于操作或保存药品不当,标签常常易损毁.现有四瓶溶液①②③④由于操作不当标签已经破损(如图),但是已经知道这四瓶溶液分别是NaOH、Ca(OH)2、Na2CO3、KCl溶液中的一种,某兴趣小组同学决定对四瓶标签破损溶液成分进行探究(只提供稀盐酸和酚酞溶液两种药品):
【提出问题】标签已经破损的①②③④四瓶溶液
分别是什么溶液?
【实验探究1】第④瓶溶液肯定是:KCl.
【实验探究2】兴趣小组对①②③三瓶溶液进行了如下的实验探究:
【反思与交流】为了防止标签发生破损,我们在倾倒溶液时应注意:倾倒药品时,标签应向手心.
 实验室由于操作或保存药品不当,标签常常易损毁.现有四瓶溶液①②③④由于操作不当标签已经破损(如图),但是已经知道这四瓶溶液分别是NaOH、Ca(OH)2、Na2CO3、KCl溶液中的一种,某兴趣小组同学决定对四瓶标签破损溶液成分进行探究(只提供稀盐酸和酚酞溶液两种药品):
实验室由于操作或保存药品不当,标签常常易损毁.现有四瓶溶液①②③④由于操作不当标签已经破损(如图),但是已经知道这四瓶溶液分别是NaOH、Ca(OH)2、Na2CO3、KCl溶液中的一种,某兴趣小组同学决定对四瓶标签破损溶液成分进行探究(只提供稀盐酸和酚酞溶液两种药品):【提出问题】标签已经破损的①②③④四瓶溶液
分别是什么溶液?
【实验探究1】第④瓶溶液肯定是:KCl.
【实验探究2】兴趣小组对①②③三瓶溶液进行了如下的实验探究:
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| (1) | 取①②③瓶溶液少量于三支试管中,分别滴入酚酞溶液 | 三瓶溶液都使无色酚酞变红色 | 不能用酚酞溶液将其中的任何一种溶液鉴别出来 |
| (2) | 再取①②③瓶溶液少量于另外三支试管中,分别滴入稀盐酸溶液 | 装有①溶液的试管中产生大量气泡;其余两支 试管中无明显现象. | ①瓶溶液是Na2CO3溶液 |
| (3) | 另取②③瓶溶液少量于另外两支试管中,分别滴入碳酸钠溶液 | 装有②溶液的试管中 无明显现象;装有③溶液的试管中产生白色沉淀 | ②瓶溶液是NaOH; ③瓶溶液是Ca(OH)2溶液 |
10.“改良环境质量,建设美丽潍坊”是我们共同的责任,下列做法不利于保护环境的是( )
| A. | 实行垃圾分类回收再利用 | |
| B. | 城市推行公共自行车制度 | |
| C. | 推广秸秆综合利用杜绝露天焚烧 | |
| D. | 为提高农作物产量可过量使用农药化肥 |
14.”神舟七号”载人宇宙飞船的太空舱为了保持舱内O2,CO2气体含量的相对稳定,使用了NiFe2O4作催化剂,将宇航员呼出的CO2转化为O2.若NiFe2O4中Fe为+3价,则Ni的化合价为( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
15.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如表
关于此反应,下列认识正确的是( )
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 7 | 1 | 21 | 10 |
| 反应后质量(g) | 待测 | 20 | 9 | 10 |
| A. | 该变化的基本反应类型是分解反应 | B. | 参加反应的甲、丙的质量比为7:12 | ||
| C. | 丁一定是该反应的催化剂 | D. | 甲反应后的质量为3g |