题目内容
14.根据下列仪器装置,回答有关问题.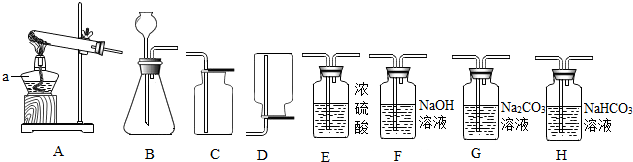
(1)制取氧气.实验室选用装置A制取氧气时,用到的化学药品是KClO3和MnO2(用化学式表示);收集氧气可以选用的装置是C填装置序号).实验结束熄灭酒精灯的操作为用灯帽盖灭(盖灭后轻提下灯帽).
(2)制取二氧化碳.用一定浓度的盐酸与石灰石反应制取二氧化碳气体,发生反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.为制得干燥、纯净的二氧化碳气体,所选装置的连接顺序为(B)→H→(E)→干燥、纯净CO2 (在括号内填装置序号).
(3)进一步探究二氧化碳与氢氧化钠溶液的反应.
【提出问题】制取干燥、纯净的二氧化碳气体流程中,选用装置H而不用G,因为碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O═2NaHCO3.向氢氧化钠溶液中通入一定量二氧化碳后,所得溶液中溶质是什么?
【查阅资料】碳酸氢钠与氢氧化钠发生反应:NaOH+NaHCO3═Na2CO3+H2O;Ca(HCO3)2溶于水.
【猜想】所得溶液中的溶质是:
①Na2CO3;②NaHCO3;③Na2CO3和NaHCO3;④Na2CO3和NaOH.
【实验】请你参与下列验证猜想③的实验,完成探究报告.
| 步骤和方法 | 现象 | 分析 |
| 取少量反应后的溶液,加入足量的CaCl2溶液 | 产生白色沉淀 | 发生反应的方程式: CaCl2+Na2CO3=CaCO3↓+2NaCl |
| 过滤,向滤液中加入少量NaOH溶液 | 产生白色沉淀 | 结论:猜想③正确 |
是通入二氧化碳的量多少.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热,加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.(1)装置A是固体加热型,且试管口无棉花,说明是用加热氯酸钾和二氧化锰混合物的方法制取氧气,氧气的密度比空气大,不易溶于水,据此选择收集装置,(2)根据石灰石和盐酸反应生成氯化钙、水和二氧化碳书写方程式,该反应属于固液常温型,故选发生装置B,干燥二氧化碳用浓硫酸.实验探究中,猜想所得溶液中的溶质是:①Na2CO3;②NaHCO3;③Na2CO3和NaHCO3;④Na2CO3和NaOH;探究报告中,取少量反应后的溶液,加入足量的CaCl2溶液,产生白色沉淀;过滤,向滤液中加入少量NaOH溶液产生白色沉淀,因为碳酸氢钠在碱性的条件下溶解度很小,结晶析出,结论:猜想③正确;二氧化碳通入一定量的氢氧化钠溶液,影响反应后生成物成分的决定因素是通入二氧化碳的量多少.
解答 解:(1)如果用氯酸钾和二氧化锰制氧气就需要加热,加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;实验结束熄灭酒精灯的操作为:用灯帽盖灭,盖灭后轻提下灯帽;故答案为:KClO3 和MnO2 C 用灯帽盖灭(盖灭后轻提下灯帽)
(2)根据石灰石和盐酸反应生成氯化钙、水和二氧化碳书写方程式,该反应属于固液常温型,故选发生装置B,干燥二氧化碳用浓硫酸;要先除杂质后干燥,故答案为:CaCO3+2HCl=CaCl2+CO2↑+H2O; B; E;
(3)【猜想】实验探究中,猜想所得溶液中的溶质是:①Na2CO3;②NaHCO3;③Na2CO3和NaHCO3;④Na2CO3和NaOH;故答案为:Na2CO3和NaOH
【实验】探究报告中,取少量反应后的溶液,加入足量的CaCl2溶液,产生白色沉淀;过滤,向滤液中加入少量NaOH溶液产生白色沉淀,因为碳酸氢钠在碱性的条件下溶解度很小,结晶析出,结论:猜想③正确;故答案为:
| 步骤和方法 | 现象 | 分析 |
| 产生白色沉淀 | CaCl2+Na2CO3=CaCO3↓+2NaCl(2分) | |
| 过滤,向滤液中加入少量NaOH溶液 |
点评 本考点主要考查了药品的选择、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和实验探究等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. |  将过量的镁和铁分别放入等质量、相同质量分数的稀盐酸中 | |
| B. |  40℃时,向一定量的硝酸钾不饱和溶液中逐渐加入硝酸钾固体 | |
| C. |  用酒精灯加热一定量的高锰酸钾固体 | |
| D. |  电解水时产生氢气与氧气的体积比 |
| 测定次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 样品质量(g) | 1000 | 1000 | 1000 | 1000 |
| 氢氧化钠溶液质量(g) | 320 | 640 | 820 | 900 |
| 沉淀质量(g) | 23.2 | 46.4 | 58 | 58 |
| A. | 汽车限购限行 | B. | 盗版光盘焚烧处理 | ||
| C. | 禁止燃放烟花泡竹 | D. | 广泛使用太阳能和风能等清洁能源 |

| A. | A是甲、乙两物质的溶解度曲线图.将t1℃时甲、乙两物质的饱和溶液升温到t2℃,两溶液的溶质质量分数都减小 | |
| B. | B图反映了某个化学反应各物质质量与时间的关系,该反应是化合反应 | |
| C. | 一定温度(t℃)时,向一定量的饱和石灰水中加入生石灰 | |
| D. | 向盐酸和氯化铁的混合溶液中加入氢氧化钠熔液 |
| A. | 检验二氧化碳中是否含有氯化氢气体,用紫色的石蕊溶液检验 | |
| B. | 除去铜粉中的氧化铜,将混合物放入稀硫酸中,过滤,洗涤,烘干 | |
| C. | 制少量氢氧化镁,将适量的氢氧化钡溶液与硫酸镁溶液混合,过滤 | |
| D. | 分离氯化钠和氯化钙,加入适量碳酸钠溶液,充分反应后,过滤,蒸发 |
 (1)我国化学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,制得纯碱(Na2CO3),Na2CO3和NaCl的溶解度曲线如图所示:
(1)我国化学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,制得纯碱(Na2CO3),Na2CO3和NaCl的溶解度曲线如图所示: