题目内容
3.下列实验方案中,设计合理的是( )| A. | 检验二氧化碳中是否含有氯化氢气体,用紫色的石蕊溶液检验 | |
| B. | 除去铜粉中的氧化铜,将混合物放入稀硫酸中,过滤,洗涤,烘干 | |
| C. | 制少量氢氧化镁,将适量的氢氧化钡溶液与硫酸镁溶液混合,过滤 | |
| D. | 分离氯化钠和氯化钙,加入适量碳酸钠溶液,充分反应后,过滤,蒸发 |
分析 A、根据二氧化碳与水反应生成碳酸、氯化氢气体均能使紫色的石蕊溶液变红色,进行分析判断.
B、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
C、根据氢氧化钡溶液与硫酸镁溶液反应生成氢氧化镁沉淀和硫酸钡沉淀,进行分析判断.
D、根据氯化钙与碳酸钠溶液反应生成碳酸钙白色沉淀和氯化钠,进行分析判断.
解答 解:A、二氧化碳与水反应生成碳酸,氯化氢气体均能使紫色的石蕊溶液变红色,不能用紫色的石蕊溶液检验,故选项实验方案设计不合理.
B、CuO能与稀硫酸反应生成硫酸铜和水,铜不与稀硫酸反应,再过滤,洗涤,烘干,可以除去杂质,故选项实验方案设计合理.
C、氢氧化钡溶液与硫酸镁溶液反应生成氢氧化镁沉淀和硫酸钡沉淀,过滤后得到的是氢氧化镁沉淀和硫酸钡沉淀的混合物,故选项实验方案设计不合理.
D、氯化钙与碳酸钠溶液反应生成碳酸钙白色沉淀和氯化钠,加入适量碳酸钠溶液,充分反应后,过滤,不能分离出氯化钙,故选项实验方案设计不合理.
故选:B.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
相关题目
4.对图所示实验现象分析正确的是( )
| A. |  实验中试管内液面上升,说明试管内压强增大 实验中试管内液面上升,说明试管内压强增大 | |
| B. |  实验中小气球迅速胀大,说明NaOH能与CO2反应 实验中小气球迅速胀大,说明NaOH能与CO2反应 | |
| C. |  实验中U型管内液面左高右低,说明NH4NO3能与水发生反应 实验中U型管内液面左高右低,说明NH4NO3能与水发生反应 | |
| D. |  实验中紫色石蕊溶液变红,说明CO2是一种酸 实验中紫色石蕊溶液变红,说明CO2是一种酸 |
14.根据下列仪器装置,回答有关问题.
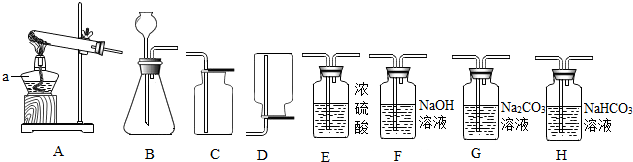
(1)制取氧气.实验室选用装置A制取氧气时,用到的化学药品是KClO3和MnO2(用化学式表示);收集氧气可以选用的装置是C填装置序号).实验结束熄灭酒精灯的操作为用灯帽盖灭(盖灭后轻提下灯帽).
(2)制取二氧化碳.用一定浓度的盐酸与石灰石反应制取二氧化碳气体,发生反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.为制得干燥、纯净的二氧化碳气体,所选装置的连接顺序为(B)→H→(E)→干燥、纯净CO2 (在括号内填装置序号).
(3)进一步探究二氧化碳与氢氧化钠溶液的反应.
【提出问题】制取干燥、纯净的二氧化碳气体流程中,选用装置H而不用G,因为碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O═2NaHCO3.向氢氧化钠溶液中通入一定量二氧化碳后,所得溶液中溶质是什么?
【查阅资料】碳酸氢钠与氢氧化钠发生反应:NaOH+NaHCO3═Na2CO3+H2O;Ca(HCO3)2溶于水.
【猜想】所得溶液中的溶质是:
①Na2CO3;②NaHCO3;③Na2CO3和NaHCO3;④Na2CO3和NaOH.
【实验】请你参与下列验证猜想③的实验,完成探究报告.
【讨论】二氧化碳通入一定量的氢氧化钠溶液,影响反应后生成物成分的决定因素
是通入二氧化碳的量多少.

(1)制取氧气.实验室选用装置A制取氧气时,用到的化学药品是KClO3和MnO2(用化学式表示);收集氧气可以选用的装置是C填装置序号).实验结束熄灭酒精灯的操作为用灯帽盖灭(盖灭后轻提下灯帽).
(2)制取二氧化碳.用一定浓度的盐酸与石灰石反应制取二氧化碳气体,发生反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.为制得干燥、纯净的二氧化碳气体,所选装置的连接顺序为(B)→H→(E)→干燥、纯净CO2 (在括号内填装置序号).
(3)进一步探究二氧化碳与氢氧化钠溶液的反应.
【提出问题】制取干燥、纯净的二氧化碳气体流程中,选用装置H而不用G,因为碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O═2NaHCO3.向氢氧化钠溶液中通入一定量二氧化碳后,所得溶液中溶质是什么?
【查阅资料】碳酸氢钠与氢氧化钠发生反应:NaOH+NaHCO3═Na2CO3+H2O;Ca(HCO3)2溶于水.
【猜想】所得溶液中的溶质是:
①Na2CO3;②NaHCO3;③Na2CO3和NaHCO3;④Na2CO3和NaOH.
【实验】请你参与下列验证猜想③的实验,完成探究报告.
| 步骤和方法 | 现象 | 分析 |
| 取少量反应后的溶液,加入足量的CaCl2溶液 | 产生白色沉淀 | 发生反应的方程式: CaCl2+Na2CO3=CaCO3↓+2NaCl |
| 过滤,向滤液中加入少量NaOH溶液 | 产生白色沉淀 | 结论:猜想③正确 |
是通入二氧化碳的量多少.
8.下列各组物质的溶液不用其他试剂就可鉴别的是( )
| A. | NaCl Na2CO3 Ca(NO3)2 HCl | |
| B. | HCl CuSO4 KNO3 Na2SO4 | |
| C. | Na2SO4 BaCl2 K2CO3 KNO3 | |
| D. | NaNO3 Na2SO4 HCl H2SO4 |
15.下列图象能正确反映相应操作过程的是( )
| A. | 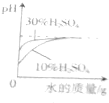 稀释等质量溶质质量分数分别为30%和10%的H2SO4溶液 | |
| B. | 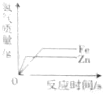 等质量的锌粉和铁粉,分别与质量分数相同的足量稀盐酸反应 | |
| C. |  在恒温条件下,将饱和的氯化钠溶液恒温蒸发水分至有白色晶体析出 | |
| D. | 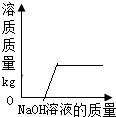 向氯化铜和硝酸铜的混合溶液中滴加氢氧化钠溶液 |
12.科学家屠呦呦因提取青蒿素(C15H22O5)而获得2015年诺贝尔奖,下列说法不正确的是( )
| A. | 青蒿素属于有机物 | |
| B. | 青蒿素的相对分子质量为282 | |
| C. | 一个青蒿素分子由15个碳原子、12个氢原子和5个水分子构成 | |
| D. | 青蒿素中碳、氢、氧三种元素的质量比为90:11:40 |

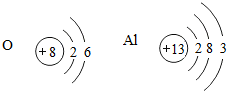 如图是氧和铝两种元素的原子结构示意图:
如图是氧和铝两种元素的原子结构示意图: