题目内容
19.硝酸银(AgNO3)是实验室常用的化学试剂,在光照或加热的条件下化学性质不稳定:2AgNO3$\frac{\underline{\;光照\;}}{\;}$2Ag+2NO2↑+X↑.(1)AgNO3中氮元素的化合价是+5;
(2)上述反应中,生成气体X的化学式为O2;
(3)实验室保存AgNO3应注意的问题是避光、密封保存.
分析 (1)根据化合物中化合价代数和为零来分析;
(2)根据化学变化前后原子的种类、数目不变,由反应的化学方程式2AgNO3$\frac{\underline{\;光照\;}}{\;}$2Ag+2NO2↑+X↑,推断反应中生成物X的分子构成,根据分子的构成确定X物质的化学式;
(3)硝酸银见光易分解变质,故应放在棕色瓶中避光保存.
解答 解:(1)设AgNO3中氮元素的化合价为x,则+1+x+(-2)×3=0,解得x=+5;
(2)根据反应的化学方程式2AgNO3$\frac{\underline{\;光照\;}}{\;}$2Ag+2NO2↑+X↑,可得知反应前后各原子的个数为:
反应前 反应后
银原子 2 2
氮原子 2 2
氧原子 6 4
根据化学变化前后原子的种类、数目不变,生成物X中有2个O原子,则物质X的化学式为O2;
(3)硝酸银见光易分解变质,故应放在棕色瓶中避光保存.
故答案为:
(1)+5;(2)O2;(3)避光、密封保存.
点评 此题是对化合价计算、化学试剂存放、金属活动性顺序的考查,解题的关键是对相关知识的掌握与应用,属于基础性知识的考查题.

练习册系列答案
相关题目
20.亮亮做家务时接触到下列用品.
(1)他清理垃圾时发现一袋脱氧剂,拆开后看到还原铁粉已生锈,铁生锈的原因是Fe与潮湿的空气接触.
(2)他选用洁厕灵清除水垢(主要成分是碳酸钙),洁厕灵pH<7(填“<”、“>”或“=”)
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
(4)做完家务,他用Vc泡腾片冲了一杯饮料.下列Vc泡腾片的主要成分中,属于有机物的是AB(填字母序号).
A.维生素C(C6H8O6) B.柠檬酸(C6H8O7) C.碳酸氢钠(NaHCO3)
| 用品 | 脱氧剂 | 洁厕灵 | 炉灶清洁剂 |
| 有效成分 | 还原铁粉 | 盐酸 | 氢氧化钠 |
(2)他选用洁厕灵清除水垢(主要成分是碳酸钙),洁厕灵pH<7(填“<”、“>”或“=”)
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
(4)做完家务,他用Vc泡腾片冲了一杯饮料.下列Vc泡腾片的主要成分中,属于有机物的是AB(填字母序号).
A.维生素C(C6H8O6) B.柠檬酸(C6H8O7) C.碳酸氢钠(NaHCO3)
14.根据下列仪器装置,回答有关问题.
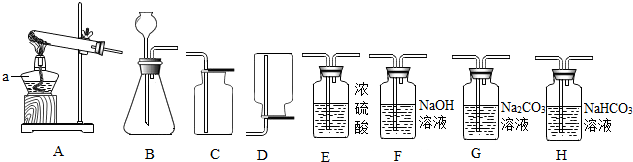
(1)制取氧气.实验室选用装置A制取氧气时,用到的化学药品是KClO3和MnO2(用化学式表示);收集氧气可以选用的装置是C填装置序号).实验结束熄灭酒精灯的操作为用灯帽盖灭(盖灭后轻提下灯帽).
(2)制取二氧化碳.用一定浓度的盐酸与石灰石反应制取二氧化碳气体,发生反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.为制得干燥、纯净的二氧化碳气体,所选装置的连接顺序为(B)→H→(E)→干燥、纯净CO2 (在括号内填装置序号).
(3)进一步探究二氧化碳与氢氧化钠溶液的反应.
【提出问题】制取干燥、纯净的二氧化碳气体流程中,选用装置H而不用G,因为碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O═2NaHCO3.向氢氧化钠溶液中通入一定量二氧化碳后,所得溶液中溶质是什么?
【查阅资料】碳酸氢钠与氢氧化钠发生反应:NaOH+NaHCO3═Na2CO3+H2O;Ca(HCO3)2溶于水.
【猜想】所得溶液中的溶质是:
①Na2CO3;②NaHCO3;③Na2CO3和NaHCO3;④Na2CO3和NaOH.
【实验】请你参与下列验证猜想③的实验,完成探究报告.
【讨论】二氧化碳通入一定量的氢氧化钠溶液,影响反应后生成物成分的决定因素
是通入二氧化碳的量多少.

(1)制取氧气.实验室选用装置A制取氧气时,用到的化学药品是KClO3和MnO2(用化学式表示);收集氧气可以选用的装置是C填装置序号).实验结束熄灭酒精灯的操作为用灯帽盖灭(盖灭后轻提下灯帽).
(2)制取二氧化碳.用一定浓度的盐酸与石灰石反应制取二氧化碳气体,发生反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.为制得干燥、纯净的二氧化碳气体,所选装置的连接顺序为(B)→H→(E)→干燥、纯净CO2 (在括号内填装置序号).
(3)进一步探究二氧化碳与氢氧化钠溶液的反应.
【提出问题】制取干燥、纯净的二氧化碳气体流程中,选用装置H而不用G,因为碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O═2NaHCO3.向氢氧化钠溶液中通入一定量二氧化碳后,所得溶液中溶质是什么?
【查阅资料】碳酸氢钠与氢氧化钠发生反应:NaOH+NaHCO3═Na2CO3+H2O;Ca(HCO3)2溶于水.
【猜想】所得溶液中的溶质是:
①Na2CO3;②NaHCO3;③Na2CO3和NaHCO3;④Na2CO3和NaOH.
【实验】请你参与下列验证猜想③的实验,完成探究报告.
| 步骤和方法 | 现象 | 分析 |
| 取少量反应后的溶液,加入足量的CaCl2溶液 | 产生白色沉淀 | 发生反应的方程式: CaCl2+Na2CO3=CaCO3↓+2NaCl |
| 过滤,向滤液中加入少量NaOH溶液 | 产生白色沉淀 | 结论:猜想③正确 |
是通入二氧化碳的量多少.
4.能在pH为1的溶液中大量共存,且溶液为无色透明的一组物质是( )
| A. | K2SO4、NaNO3、NH4C1 | B. | FeCl3、CuSO4、NaCl | ||
| C. | BaCl2、Na2SO4、NaOH | D. | CaCl2、Na2CO3、AgNO3 |
8.下列各组物质的溶液不用其他试剂就可鉴别的是( )
| A. | NaCl Na2CO3 Ca(NO3)2 HCl | |
| B. | HCl CuSO4 KNO3 Na2SO4 | |
| C. | Na2SO4 BaCl2 K2CO3 KNO3 | |
| D. | NaNO3 Na2SO4 HCl H2SO4 |
9.当前,世界已经迈向了“低碳”时代,选择“低碳”既是一种生活方式也是一种生存责任.曲阜市公交系统适应形势发展,推广使用节能减排的双燃料公交车.如图为公交车燃料主要成分完全燃烧的化学反应的微观示意图.下列说法中正确的是( )


| A. | 物质甲的化学式是CH4 | |
| B. | 该反应中分子和原子的种类都发生了改变 | |
| C. | 甲、乙两物质参加反应的质量比为1:2 | |
| D. | 图示反应属于复分解反应 |

