题目内容
8.2015年12月,上合会议在郑州召开,李克强总理用河南烩面招待了各国首脑政要,河南烩面配料(面粉、羊肉、食盐、青菜等)重含有的营养素有蛋白质、糖类(写两种),加碘食盐所含KIO3中I显+5价.分析 根据人体所需六大营养素的种类、食物来源,结合题中所给的食物判断所含的营养素,进行分析解答;根据化合物中各元素化合价代数和为零的原则进行分析解答.
解答 解:面粉中主要含有糖类;羊肉中主要含有蛋白质;食盐属于无机盐;青菜中主要含有维生素;因为化合物中元素化合价的代数和为0,设化合物KIO3中I元素化合价为n价,依化合物中各元素化合价代数和为零的原则,有(+1)+n+(-2)×3=0,解得n=+5;
故答案为:蛋白质、糖类等;+5.
点评 化学来源于生产生活,也服务于生产生活,因此在近年的中考中,与生产生活实际相关的情景题已渐渐成为新宠.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
5.下列各物质在水中能大量共存的是( )
| A. | NaCl、Na2CO3、KNO3 | B. | Ca(OH)2、KCl、K2CO3 | ||
| C. | H2SO4、Na2SO4、NaOH | D. | CuSO4、NaOH、Na2SO4 |
16.某化学兴趣小组的同学将足量镁带投入NH4Cl溶液中,发现镁带逐渐溶解的同时有较多的气泡放出,镁能与NH4Cl溶液反应吗?如果能反应,生成物可能是什么?同学们进行下列实验探究:
探究1:反应后所得溶液中溶质是什么?
【进行猜想】可能是MgCl2
【实验验证】
探究2:反应后生成的气体是什么?
【进行猜想】猜想一:可能是NH3;
猜想二:可能是氢气;
猜想三:可能是NH3和H2的混合气体;
【查阅资料】在百度网页中输入氨气的化学性质,可以获知氨气的部分化学性质如下:
①跟谁反应:NH3+H2O═NH3•H2O
②跟酸反应:NH3+HCl═NH4Cl 2NH3+H2SO4═(NH4)2SO4
③跟某些金属氧化物反应:3CuO+2NH3$\frac{\underline{\;△\;}}{\;}$3Cu+3H2O+N2
【实验探究】为了探究气体的成分,同学们设计了如下实验装置:
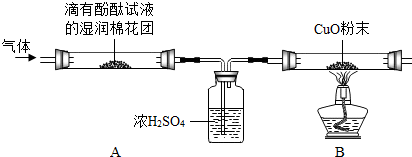
①A中观察到A中棉花团变红色,证明有NH3;
②B中玻璃管内观察到黑色粉末变红色,证明有H2;
③浓硫酸的作用是吸收氨气.
【实验结论】综合以上实验现象和分析,镁与NH4Cl反应的化学方程式为Mg+2NH4Cl=MgCl2+H2↑+2NH3↑.
探究1:反应后所得溶液中溶质是什么?
【进行猜想】可能是MgCl2
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 |
| 取反应后溶液少量于试管中,滴入NaOH溶液 | 产生白色沉淀 | 反应后所得溶液中溶质是MgCl2 |
| 另取反应后溶液少量于试管中,滴入硝酸银溶液和稀硝酸. |
【进行猜想】猜想一:可能是NH3;
猜想二:可能是氢气;
猜想三:可能是NH3和H2的混合气体;
【查阅资料】在百度网页中输入氨气的化学性质,可以获知氨气的部分化学性质如下:
①跟谁反应:NH3+H2O═NH3•H2O
②跟酸反应:NH3+HCl═NH4Cl 2NH3+H2SO4═(NH4)2SO4
③跟某些金属氧化物反应:3CuO+2NH3$\frac{\underline{\;△\;}}{\;}$3Cu+3H2O+N2
【实验探究】为了探究气体的成分,同学们设计了如下实验装置:

①A中观察到A中棉花团变红色,证明有NH3;
②B中玻璃管内观察到黑色粉末变红色,证明有H2;
③浓硫酸的作用是吸收氨气.
【实验结论】综合以上实验现象和分析,镁与NH4Cl反应的化学方程式为Mg+2NH4Cl=MgCl2+H2↑+2NH3↑.
3.2015年6月5日是第44个“世界环境日”,也是我国新《环保法》实施后的首个“环境日”,我国今年的主题是“践行绿色生活”,下列做法符合这一主题的是( )
| A. | 将农田中产生的秸秆就地焚烧 | B. | 将废旧电池深埋 | ||
| C. | 高炉炼铁的废气直接排放到大气中 | D. | 增加植树造林面积 |
20.如图是工业生产水煤气的化学反应微观示意图,有关叙述错误的是( )
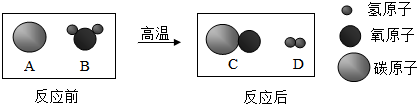

| A. | 该反应是置换反应 | B. | 图中气体单质的化学式为H2 | ||
| C. | 反应后原子的个数减少 | D. | 水煤气泄漏会污染空气 |
17.证据是科学探究中获得结论的重要的依据.让我们一起经历一次寻找证据的旅程吧.
【实验目的】制取纯净的硫酸钡(反应原理:Na2SO4+BaCl2═BaSO4↓+2NaCl)
【实验步骤】取一定量的硫酸钠和氯化钡溶液反应,过滤、洗涤、干燥得到纯净的硫酸钡.
(1)实验中,能直接观察到说明硫酸钠和氯化钡溶液发生化学反应的证据是:有白色沉淀生成.
(2)判断任一反应物是否完全反应的证据可按如下方法获取:
(3)如果实验证明氯化钡已经反应完全,要寻找硫酸钡已纯净的证据,我们可以从证明实
验制得的硫酸钡中没有氯化钠(填具体物质)来设计实验方案.
【实验目的】制取纯净的硫酸钡(反应原理:Na2SO4+BaCl2═BaSO4↓+2NaCl)
【实验步骤】取一定量的硫酸钠和氯化钡溶液反应,过滤、洗涤、干燥得到纯净的硫酸钡.
(1)实验中,能直接观察到说明硫酸钠和氯化钡溶液发生化学反应的证据是:有白色沉淀生成.
(2)判断任一反应物是否完全反应的证据可按如下方法获取:
| 猜想 | 方案 | 证据 | 结论 |
| 氯化钡可能已 完全反应 | 取少量滤液,加入稀硫酸 溶液,观察现象 | 无白色沉淀生成 | 氯化钡已完全反应 |
| 硫酸钠可能已 完全反应 | 无白色沉淀生成 | 硫酸钠未完全反应 |
验制得的硫酸钡中没有氯化钠(填具体物质)来设计实验方案.
18.下列有关描述中,不正确的是( )
| A. | 清理沼气池前做灯火实验 | B. | 进入山洞时用火把照明 | ||
| C. | 煮沸能降低水的硬度 | D. | 天然气泄漏,立即关闭阀门 |