题目内容
18.下列实验方案中,正确的是( )| A. | 除去氧化钙中混有的少量的碳酸钙:用过量稀盐酸 | |
| B. | 鉴别稀盐酸、NaCl和KOH三种无色溶液:取样,分别滴加酚酞溶液 | |
| C. | 除去O2中含有的少量水蒸气和CO2:将混合气体依次通过烧碱溶液和浓硫酸 | |
| D. | 分离NaCl和BaCl2:先加适量的Na2CO3溶液,过滤后向固体中再加稀硫酸 |
分析 A、根据盐酸能够与碳酸钙和氧化钙两种物质均能反应分析解答;
B、根据稀盐酸、NaCl溶液和KOH溶液三种溶液的酸碱性不同分析解答;
C、根据除去O2中含有的少量水蒸气和CO2,要先除二氧化碳,后除水蒸气,进行分析判断;
D、要分离氯化钠和氯化钡的混合溶液,可以加入合适的试剂使其中的一种物质转化为沉淀,然后再加入试剂使其转化为原来的物质.
解答 解:A、盐酸与碳酸钙反应和氧化钙也能反应,所以加稀盐酸虽能够除掉碳酸钙,但也会反应掉氧化钙,故该方法不可行;
B、稀盐酸显酸性,NaCl显中性,KOH溶液显碱性,取样,分别滴加酚酞溶液,变红的是氢氧化钾溶液,不变红的是稀盐酸和氯化钠溶液,所以用该方法不可以鉴别三者;
C、除去O2中含有的少量水蒸气和CO2,将混合气体先通过烧碱溶液除去二氧化碳气体,然后将含有少量水蒸气的氧气再通过浓硫酸除去水蒸气,故该方案可行;
D、要分离NaCl和BaCl2的混合溶液,可以先加入碳酸钠溶液与氯化钡反应生成碳酸钡沉淀,然后过滤出的沉淀加入盐酸与生成的碳酸钡反应生成氯化钡即可,不能加稀硫酸,故该方案不可行;
故选C.
点评 本题难度不大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
相关题目
3.如图中两圆相交部分表示物质间反应的主要实验现象,下列说法中正确的是( )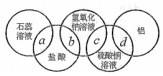

| A. | a处溶液呈蓝色 | |
| B. | b处反应后溶液的总质量增加 | |
| C. | c处产生白色沉淀 | |
| D. | d处银白色固体表面有红色固体析出 |
9.如图,加入水后,U形管中的液面左升右降,X可能是下列物质中的( )


| A. | NH4NO3 | B. | NaOH | C. | CaO | D. | NaCl |
13.下列说法错误的是( )
| A. | 用食醋作调味剂 | B. | 碳酸氢钠用于治疗胃酸过多 | ||
| C. | 食品中禁止使用防腐剂 | D. | 用布袋代替塑料袋减少白色污染 |
3.下列变化过程中,只发生物理变化的是( )
| A. | 食物变质 | B. | 纸张燃烧 | C. | 酒精挥发 | D. | 钢铁生锈 |
10.下列实验方案中,合理的是( )
| A. | 实验室制备H2:用足量的锌粒和稀盐酸混合充分反应 | |
| B. | 鉴别Na2CO3溶液和NaOH溶液:取样,分别加酚酞溶液 | |
| C. | 除去N2中混有的CO:将混合气体通过灼热的CuO粉末 | |
| D. | 验证NaOH溶液与稀盐酸反应:取反应后溶液滴加CuSO4溶液 |
8.科学推理是研究和学习化学的一种重要方法,下列推理正确的是( )
| A. | 点燃氢气前要检验纯度,所以点燃一氧化碳前也要检验纯度 | |
| B. | 燃烧一般都伴随发光、放热的现象,所以有发光、放热现象的变化就是燃烧 | |
| C. | CO2通入紫色石蕊试液,溶液变成红色,说明CO2呈酸性 | |
| D. | 饱和食盐水中不能再溶解食盐,也一定不能再溶解蔗糖 |
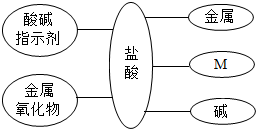 构建思维图,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的思维图.结合此图回答下列问题:
构建思维图,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的思维图.结合此图回答下列问题: 2016年9月18日,众余氢能技术有限公司就发布了一款氢能源大巴产品,据悉,该大巴所采用的是氢燃料电池.目前国内其他厂家生产的氢能源汽车燃料电池动力系统全部采用进口设备,这一技术填补了国内氢燃料电池动力系统的空白.请回答有关问题:
2016年9月18日,众余氢能技术有限公司就发布了一款氢能源大巴产品,据悉,该大巴所采用的是氢燃料电池.目前国内其他厂家生产的氢能源汽车燃料电池动力系统全部采用进口设备,这一技术填补了国内氢燃料电池动力系统的空白.请回答有关问题: