题目内容
12.经测定,在任何水溶液中,均存在一定数量的H+〔用n(H+)表示〕和一定数量的OH-〔用n(OH-)表示〕,n(H+)与n(OH-)的相对大小对应溶液的酸碱性如表所示:| n(H+)与n(OH-)的相对大小 | 溶液的酸碱性 |
| n(H+)>n(OH-) | 酸性 |
| n(H+)=n(OH-) | 中性 |
| n(H+)<n(OH-) | 碱性 |
(1)常温下测得水中pH=7,可知水中n(H+)=n(OH-)(填“>”或“=”或“<”).
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是溶液变为红色,再往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+)>n(OH-)(填“>”或“=”或“<”).
分析 溶液的酸碱性是根据溶液中H+浓度与OH-浓度的相对大小判断.
(1)根据常温下测得水中pH=7,溶液为中性解答;
(2)根据酚酞溶液遇碱性溶液变红,碳酸钠溶液呈碱性解答,根据实验现象分析解答.
解答 解:溶液的酸碱性是根据溶液中H+浓度与OH-浓度的相对大小判断.
当[H+]=[OH-],溶液就呈中性;
当[H+]>[OH-],溶液就呈酸性,且[H+]越大酸性越强;
当溶液中[H+]<[OH-],溶液就呈碱性,且[OH-]越大碱性越强.
(1)常温下测得水中pH=7,溶液为中性,可知水中n(H+)=n(OH-);
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是溶液变为红色,往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明碱性减弱,硫酸氢钠溶液中n(H+)>n(OH-).
故答案为:
(1)=;
(2)溶液变为红色;>
点评 本题主要考查溶液的酸碱性的判断,注意不能根据溶液的PH值判断溶液的酸碱性,要根据氢离子浓度和氢氧根离子浓度的相对大小判断溶液的酸碱性.

练习册系列答案
相关题目
2.把100g溶质质量分数为10%的食盐溶液稀释成2%的食盐溶液,不需要用到的仪器是( )
| A. | 量筒 | B. | 烧杯 | C. | 玻璃棒 | D. | 托盘天平 |
3.如图为某反应在同一容器中反应前后微粒示意图.下列说法不正确的是( )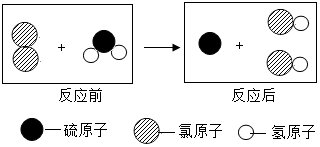

| A. | 化学反应前后分子保持不变 | B. | 该反应的化学式为Cl2+H2S=S+HCl | ||
| C. | 该反应为置换反应 | D. | 原子是化学变化中的最小粒子 |
20.下列物质的除杂实验中,所选用的试剂、方法及反应类型均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂、方法 | 反应类型 |
| A | CaCO3(CaO) | 高温 | 分解反应 |
| B | Fe(Fe2O3) | 足量CO | 置换反应 |
| C | CO2(CO) | 足量O2 | 化合反应 |
| D | CaCl2溶液(HCl) | 足量CaCO3 | 复分解反应 |
| A. | A | B. | B | C. | C | D. | D |
7.正确的实验操作是科学探究成功的基础,下列操作中正确的是( )
| A. |  倾倒液体 | B. |  氢气还原氧化铜 | ||
| C. |  取用少量液体 | D. |  稀释浓硫酸 |
18.下列有关物质构成的说法不正确的是( )
| A. | 物质可由分子、原子或离子构成 | |
| B. | 结构示意图为  、 、 的粒子,表示了同种元素的不同粒子 的粒子,表示了同种元素的不同粒子 | |
| C. | 相对原子质量为m的原子M,核外有n个电子,则核内中子数近似为:m-n | |
| D. |  所表示的原子,属于非金属元素原子 所表示的原子,属于非金属元素原子 |

 为了探究质量守恒定律,设计了如图“白磷燃烧前后质量测定”的实验,请分析有关问题:
为了探究质量守恒定律,设计了如图“白磷燃烧前后质量测定”的实验,请分析有关问题: