题目内容
5.下列化学用语表达错误的是( )| A. | 两个铁原子:2Fe | B. | 2个钙离子:2Ca2+ | ||
| C. | 硫的元素符号为:S | D. | 氢气中氢元素的化合价为+1价 |
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:A、两个铁原子表示为2Fe,正确;
B、2个钙离子表示为2Ca2+,正确;
C、硫元素的符号为S,正确;
D、氢气是单质,其中氢元素的化合价为0,错误;
故选D.
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
相关题目
15.有三种金属X、Y、Z,它们与酸或碱溶液可以发生如下反应:①Y+X(NO3)2=Y(NO3)2+X②X+H2SO4=XSO4+H2↑③Z不与盐酸反应.则该三种金属的活动性顺序为( )
| A. | X>Y>Z | B. | Y>Z>X | C. | Y>X>Z | D. | Z>Y>X |
16.为测定石灰石钙元素的质量分数,某同学取一定量该石灰石(杂质不含钙元素且不参加反应也不溶于水)研碎后直接煅烧一段时间后,称量剩余固体的质量为103g,向其加入500g质量分数为14.6%的稀盐酸恰好完全反应,过滤后称量剩余固体质量为25g,则该石灰石中钙元素的质量分数为( )
| A. | 28% | B. | 32% | C. | 40% | D. | 50% |
13.下列图示的实验操作能达到对应目的是( )
| A. | 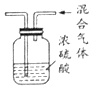 除去氧气中的水蒸气 | B. | 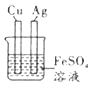 验证Fe、Cu、Ag的金属活动性强弱 | ||
| C. | 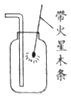 检验O2是否收集满 | D. | 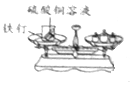 验证质量守恒定律 |
20.分类是学习和研究化学的常用方法.下列物质分类正确的是( )
| A. | 导体:石墨、铜丝、食盐水溶液 | B. | 盐类:烧碱、纯碱、小苏打 | ||
| C. | 混合物:合金、冰水共存物、碘酒 | D. | 非晶体:石蜡、海波、玻璃 |
10.下列过程中只发生物理变化的是( )
| A. | 食品的腐败 | B. | 自然界中的碳、氧循环 | ||
| C. | 蔗糖溶于水 | D. | 手机电池的充电过程 |
17.下列有关厨房里的说法正确的是( )
| A. | 切菜的刀钝了要磨一磨-为了减小压强 | |
| B. | 铝制品耐腐蚀-铝的化学性质稳定 | |
| C. | 揭开正在煮东西的锅盖时,会看到“白气”-气体的液化 | |
| D. | 煮粥时纯碱放多了加醋调节-发生了中和反应 |
15.很多水龙头是铜质镀铬的,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,同学们进行如下探究活动:
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
【回答问题】(1)用砂纸打磨金属片的目的是除去表面的氧化物.
(2)实验一所发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是铝和铬都能够和硫酸铜反应,无法比较铬和铝的金属活动性强弱.
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是A1、CrSO4溶液、Cu.
【归纳】比较金属活动性强弱的方法有
①通过金属与酸反应快慢判断金属活动性强弱
②通过金属与盐溶液反应判断金属活动性强弱.
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
| 实验一 | 实验二 | 实验三 | |
| 实验 方案 |  |  |  |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | 铜片无明显现象 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝能和稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是铝、铬、铜 | |||
(2)实验一所发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是铝和铬都能够和硫酸铜反应,无法比较铬和铝的金属活动性强弱.
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是A1、CrSO4溶液、Cu.
【归纳】比较金属活动性强弱的方法有
①通过金属与酸反应快慢判断金属活动性强弱
②通过金属与盐溶液反应判断金属活动性强弱.