题目内容
10.铬(Cr)因为具有许多神奇的性能而越来越引起人们的关注.某化学兴趣小组对Mg、Cr、Ag的金属活动性顺序进行探究.提出假设:
猜想a.金属活动性Cr>Mg>Ag;
猜想b.金属活动性Mg>Cr>Ag;
猜想c.金属活动性Mg>Ag>Cr;
查阅资料:
1、在相同条件下,金属与酸反应,产生气泡的速度越快,则该金属活动性越强.
2、铬与盐酸反应生成绿色的CrCl2溶液
实验设计:同温下,取大小相同的这三种金属薄片,分别投入等体积、等质量分数的足量稀盐酸中,观察现象.
请回答:
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是除去表面的氧化物.
(2)根据下表中的实验现象填空:
| 物 质 | Cr | Mg | Ag |
| 实验现象 | 产生气泡速度缓慢 | 产生气泡速度快 | 无任何现象 |
(3)用另一种思路设计实验证明上述结论.
| 操作 | 将Ag片放入氯化铬溶液中 | 将铬放入氯化镁溶液中 |
| 现象 | 无明显现象 | 无明显现象 |
| 结论 | Cr>Ag | Mg>Cr |
分析 根据已有的知识进行分析解答,在金属活动性顺序中,氢前的金属能与酸反应产生氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此解答.
解答 解:根据三种金属中镁的活动性强于银,还可以猜想为:Mg>Cr>Ag;故填:Mg>Cr>Ag;
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,是为了除去表面的氧化物,故填:除去表面的氧化物.
(2)铬在盐酸中缓慢产生气泡,镁在盐酸中产生气泡速度快,说明镁和铬在氢前,且镁的活动性强于铬,银在盐酸中无任何现象,说明银在氢后,故金属活动性顺序为Mg>Cr>Ag,故猜想b正确,故填:b;
(3)还可以利用金属与盐溶液是否反应验证金属的活动性顺序,故可以将银放入氯化铬溶液中,无现象,说明铬的活动性强于银,将铬放入氯化镁溶液中没有现象,说明镁的活动性强于铬,故填:
| 操作 | 将Ag片放入 氯化铬溶液中 | 将 铬放入 氯化镁溶液中 |
| 现象 | 无明显现象 | 无明显现象 |
| 结论 | Cr>Ag | Mg>Cr |
点评 本题考查的是金属活动性顺序的探究,完成此题,可以依据已有的金属活动性顺序的意义进行.

练习册系列答案
相关题目
19.下列物质属于碱的是( )
| A. | 苛性钠 | B. | 食盐 | C. | 生石灰 | D. | 石灰石 |
20.有些元素符号表示①表示一种元素 ②表示一种原子 ③表示一种单质,下列符号不具有上述三种意义的是( )
| A. | Cu | B. | He | C. | S | D. | N |
5.小明通过学习知道Na2CO3、NaHCO3均能与盐酸反应,Na2CO3溶液还会与石灰水反应.
【产生疑问】NaHCO3溶液也能与石灰水反应吗?如果能反应,生成物可能是什么?
【查阅资料】NaHCO3溶液呈碱性,CaCl2溶液呈中性,Ca(HCO3)2能溶于水,NaHCO3在碱溶液中会反应生成碳酸盐;
【进行实验】

白色沉淀A是CaCO3(填化学式),由此证明NaHCO3溶液与石灰水也能发生反应.为了进一步了解滤液生成的含钠化合物有什么,继续探究:
【作出猜想】①只有NaOH ②只有Na2CO3 ③有Na2CO3和NaOH
【实验设计】可供选择的药品:盐酸、食盐水、Ca(OH)2溶液、CaCl2溶液、酚酞试液、NaOH溶液、Na2CO3溶液、CO2气体
为了进一步验证猜想②或③,将步骤①所得液体静置后,取上层清液进行下列实验:
【拓展反思】若猜想①成立,则此时NaHCO3溶液与石灰水反应的化学方程式Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O.
【产生疑问】NaHCO3溶液也能与石灰水反应吗?如果能反应,生成物可能是什么?
【查阅资料】NaHCO3溶液呈碱性,CaCl2溶液呈中性,Ca(HCO3)2能溶于水,NaHCO3在碱溶液中会反应生成碳酸盐;
【进行实验】

白色沉淀A是CaCO3(填化学式),由此证明NaHCO3溶液与石灰水也能发生反应.为了进一步了解滤液生成的含钠化合物有什么,继续探究:
【作出猜想】①只有NaOH ②只有Na2CO3 ③有Na2CO3和NaOH
【实验设计】可供选择的药品:盐酸、食盐水、Ca(OH)2溶液、CaCl2溶液、酚酞试液、NaOH溶液、Na2CO3溶液、CO2气体
| 步骤 | 操作 | 现 象 | 结 论 |
| ① | 取少量滤液B于试管中,再滴加足量的CaCl2溶液溶液 | 如果观察到无沉淀 | 则猜想①成立. |
| 如果观察到有沉淀, | 则猜想②或③成立 |
| 步骤 | 操作 | 现 象 | 结 论 |
| ② | 取少量清液于试管中,加入足量的盐酸 | 整个实验过程无气泡产生 | 说明滤液B中无未反应完的NaHCO3 |
| ③ | 取少量清液于试管中,加入酚酞试液 | 如果观察到溶液变红色, | 则猜想③成立 |
| 如果无明显现象 | 则猜想②成立 |
15.某化学兴趣小组用如图装置完成木炭还原氧化铜的实验,并对生成的红色固体成分进行探究.
【提出问题】木炭与氧化铜反应生成的红色固体中含有什么物质?
【查阅资料】木炭与氧化铜反应也可能生成氧化亚铜(Cu2O):氧化亚铜是红色固体,能与稀硫酸反应:Cu2O+H2SO4═Cu+CuSO4+H2O.
【进行猜想】木炭与氧化铜反应生成的红色固体成分:
①全部是铜;
②全部是氧化亚铜;
③是两者的混合物.
【实验探究】
(1)用图1装置完成木炭还原氧化铜的实验,观察到澄清石灰水变浑浊,写出该反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
(2)试管冷却后,观察到黑色固体全部变为红色,对生成的红色固体成分进行探究:
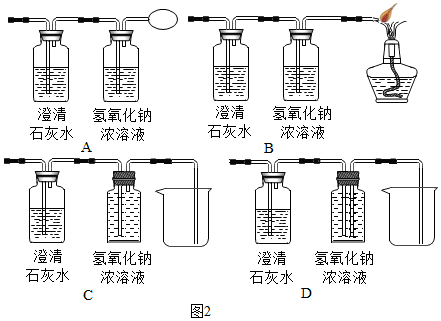
【反思与评价】木炭还原氧化铜的实验中,生成的气体可能含有一氧化碳,为了防止对空气造成污染,可将图1虚线方框内的装置改为图2中的ABD(选填字母).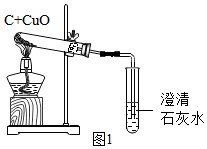
【提出问题】木炭与氧化铜反应生成的红色固体中含有什么物质?
【查阅资料】木炭与氧化铜反应也可能生成氧化亚铜(Cu2O):氧化亚铜是红色固体,能与稀硫酸反应:Cu2O+H2SO4═Cu+CuSO4+H2O.
【进行猜想】木炭与氧化铜反应生成的红色固体成分:
①全部是铜;
②全部是氧化亚铜;
③是两者的混合物.
【实验探究】
(1)用图1装置完成木炭还原氧化铜的实验,观察到澄清石灰水变浑浊,写出该反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
(2)试管冷却后,观察到黑色固体全部变为红色,对生成的红色固体成分进行探究:
| 步骤 | 现象 | 结论 |
| ①取1.8g红色固体于试管中,滴加足量稀硫酸,充分反应 | 溶液由无色变蓝色 | 猜想①错误 |
| ②过滤,将滤渣洗涤、干燥、称量 | 所得固体质量大于0.8g | 猜想③正确 |