题目内容
2.在做氢气还原氧化铜实验之后,同学们发现了试管壁上留下了一层红色的物质,老师说这层红色的物质很难除去.(1)上面所提到的“红色物质”指的是铜.
(2)为了出去这层红色物质,小华和小书分别设计了一种方案去除这种物质.
小华:在试管中加入稀硫酸,用试管刷洗刷.
小书:将试管在酒精灯上灼烧,冷却后加入稀硫酸.
你认为小书的方法可以除去红色物质.
分析 (1)根据反应的原理来分析;
(2)根据金属的活动性以及酸的性质来分析.
解答 解:(1)在加热的条件下,氢气能将氧化铜还原为红色的金属铜,同时生成水,所以这里的红色物质是指金属铜;故填:铜;
(2)铜是一种不活泼的金属,与稀硫酸不反应,故小华的方法是错误的;而在加热时,铜与空气中的氧气反应生成了氧化铜,氧化铜与稀硫酸反应生成硫酸铜和水,所以小书的方法是正确的;故填:小书.
点评 本题考查了氢气还原氧化铜的原理以及金属和酸的性质,难度不大.

练习册系列答案
相关题目
12.有关下列四种粒子的结构示意图,说法正确的是( )


| A. | 它们表示四种不同的元素 | |
| B. | ②表示的元素在化合物中通常显+2价 | |
| C. | ①③④表示的元素都是非金属元素 | |
| D. | ②③表示的元素具有相似的化学性质 |
10.铬(Cr)因为具有许多神奇的性能而越来越引起人们的关注.某化学兴趣小组对Mg、Cr、Ag的金属活动性顺序进行探究.
提出假设:
猜想a.金属活动性Cr>Mg>Ag;
猜想b.金属活动性Mg>Cr>Ag;
猜想c.金属活动性Mg>Ag>Cr;
查阅资料:
1、在相同条件下,金属与酸反应,产生气泡的速度越快,则该金属活动性越强.
2、铬与盐酸反应生成绿色的CrCl2溶液
实验设计:同温下,取大小相同的这三种金属薄片,分别投入等体积、等质量分数的足量稀盐酸中,观察现象.
请回答:
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是除去表面的氧化物.
(2)根据下表中的实验现象填空:
结论:原猜想中b正确(填“a”或“b”或“c”).
(3)用另一种思路设计实验证明上述结论.
提出假设:
猜想a.金属活动性Cr>Mg>Ag;
猜想b.金属活动性Mg>Cr>Ag;
猜想c.金属活动性Mg>Ag>Cr;
查阅资料:
1、在相同条件下,金属与酸反应,产生气泡的速度越快,则该金属活动性越强.
2、铬与盐酸反应生成绿色的CrCl2溶液
实验设计:同温下,取大小相同的这三种金属薄片,分别投入等体积、等质量分数的足量稀盐酸中,观察现象.
请回答:
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是除去表面的氧化物.
(2)根据下表中的实验现象填空:
| 物 质 | Cr | Mg | Ag |
| 实验现象 | 产生气泡速度缓慢 | 产生气泡速度快 | 无任何现象 |
(3)用另一种思路设计实验证明上述结论.
| 操作 | 将Ag片放入氯化铬溶液中 | 将铬放入氯化镁溶液中 |
| 现象 | 无明显现象 | 无明显现象 |
| 结论 | Cr>Ag | Mg>Cr |
14.把下列物质分别放入水中,成分搅拌,可以得到溶液的是( )
| A. | 花生油 | B. | 面粉 | C. | 汽油 | D. | 蔗糖 |
11.下列各组物质的变化中,前者属于化学变化,后者属于物理变化的是( )
| A. | 冰雪融化;粮食酿酒 | B. | 钢铁生锈;由熟石灰制烧碱 | ||
| C. | 蜡烛燃烧;干冰升华 | D. | 汽油挥发;食物腐烂 |
12.下列变化中,属于化学变化的是( )
| A. | 冰雪融化 | B. | 酒精挥发 | C. | 食物腐烂 | D. | 泥水沉淀 |
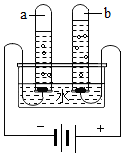 如图是水通电分解的示意图.
如图是水通电分解的示意图.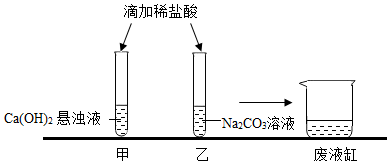 小徐同学做了如图所示的两个实验.
小徐同学做了如图所示的两个实验.