题目内容
5.高纯度的CuO可作用颜料、有机合成催化剂等.以下是用粗铜粉氧化法生产高纯度CuO的流程图(说明:所加的试剂均过量)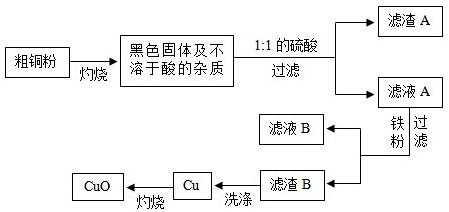
(1)1:1的H2SO4是用1体积98%的H2SO4与1体积水混合而成.配制该硫酸溶液所需的玻璃仪器除玻璃棒外,还需要烧杯、量筒.
(2)写出用硫酸溶解黑色固体的化学方程式CuO+H2SO4═CuSO4+H2O.
(3)在洗涤操作中,用H2SO4(写试剂的化学式)洗涤滤渣B.
(4)若不考虑生产过程中的损耗,要计算粗铜粉中Cu的含量,需要测定的数据是:最终所得氧化铜的质量和粗铜粉的质量(用文字表示).
分析 (1)配制1:1的硫酸溶液所需的玻璃仪器除玻璃棒外,还需要烧杯、量筒,利用量筒可以量取一定量的液体.
(2)氧化铜和稀硫酸反应生成硫酸铜和水;
(3)滤渣B中含有铜和过量的铁粉,铁能和稀硫酸反应生成硫酸亚铁和氢气;
(4)知道氧化铜的质量,可以计算铜元素的质量,铜元素质量和粗铜粉质量的比值即为粗铜粉中Cu的含量.
解答 解:(1)1:1的H2SO4是用1体积98%的H2SO4与1体积水混合而成.配制该硫酸溶液所需的玻璃仪器除玻璃棒外,还需要烧杯、量筒.
故填:量筒.
(2)黑色固体是氧化铜,和稀硫酸反应的化学方程式为:CuO+H2SO4═CuSO4+H2O.
故填:CuO+H2SO4═CuSO4+H2O.
(3)在洗涤操作中,可以用稀硫酸洗涤滤渣B,滤渣知道铁能和稀硫酸反应,铜不能和稀硫酸反应.
故填:H2SO4.
(4)若不考虑生产过程中的损耗,要计算粗铜粉中Cu的含量,需要测定的数据是:最终所得氧化铜的质量和粗铜粉的质量.
故填:粗铜粉的质量.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.实验和生产过程应尽量减少对环境的负面作用.以下符合这一思想的是( )
| A. | 实验室中氯化钡废液可直接排入下水道 | |
| B. | 利用2Cu+O2+2H2SO4(稀)═2CuSO4+2H2O的反应由铜制取胆矾 | |
| C. | 在煤矿附近建发电厂有利于减少二氧化硫排放 | |
| D. | 用废旧塑料制食品包装袋以减少“白色污染” |
13.常温常压下,10mL某气态物质含有2.68×1020个原子,则判断该物质是一种( )
| A. | 单质 | B. | 化合物 | ||
| C. | 混合物 | D. | 以上选项都有可能 |
20.碱式碳酸铜是一种用途广泛的化工原料.工业上可用电子工业中刻蚀线路板的酸性废液(主要成分有FeCl3、CuCl2、FeCl2)制备.
【工业制备】

【资料查询】:1 反应A中氯酸钠的作用是将FeCl2氧化成FeCl3
2Cu2+、Fe3+生成沉淀时的pH如下:
(1)滤渣的主要成分是Fe (OH)3(写化学式).
(2)调节反应A后溶液的pH范围应为3.2~4.2.
(3)反应B的温度如过高,则所得蓝绿色产品中可能会出现的黑色固体是CuO(写化学式).
(4)过滤得到的产品可用蒸馏水洗涤,为检验是否洗涤干净,可取最后一次洗涤液,先加入硝酸银溶液,再滴加稀硝酸,观察到不产生白色沉淀 则表明已洗净.
【组成测定】碱式碳酸铜的组成可表示为:aCuCO3•bCu(OH)2•cH2O.某研究小组设计如图2实验装置.
【资料查询】:CuCO3、Cu(OH)2受热易分解,各生成对应的两种氧化物.
充分反应后测得:①A中样品质量为12.0g,②A中剩余固体质量为8.0g,③B装置增重1.8g,④C装置增重2.2g.(各装置均充分吸收,不考虑装置中空气的影响)
(5)B中的试剂是c,C中的试剂是d,D中的试剂是a(填字母序号);
a.碱石灰 b.浓硫酸 c.无水硫酸铜 d.浓NaOH溶液
(6)计算得出样品的组成,只需实验测得四个数据中的三个即可,则可行的组合为abcd(填序号,多选少选不给分).
a.②③④b.①③④c.①②④d.①②③
通过计算可得碱式碳酸铜(aCuCO3•bCu(OH)2•cH2O)中a:b:c=1:1:1.
(7)D的作用防止空气中的二氧化碳进入C中.若将D装置去掉,a值将偏大(填“偏大”、“偏小”或“不变”)
【工业制备】

【资料查询】:1 反应A中氯酸钠的作用是将FeCl2氧化成FeCl3
2Cu2+、Fe3+生成沉淀时的pH如下:
| 物 质 | Cu(OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 1.2 |
| 完全沉淀pH | 6.7 | 3.2 |
(2)调节反应A后溶液的pH范围应为3.2~4.2.
(3)反应B的温度如过高,则所得蓝绿色产品中可能会出现的黑色固体是CuO(写化学式).
(4)过滤得到的产品可用蒸馏水洗涤,为检验是否洗涤干净,可取最后一次洗涤液,先加入硝酸银溶液,再滴加稀硝酸,观察到不产生白色沉淀 则表明已洗净.
【组成测定】碱式碳酸铜的组成可表示为:aCuCO3•bCu(OH)2•cH2O.某研究小组设计如图2实验装置.
【资料查询】:CuCO3、Cu(OH)2受热易分解,各生成对应的两种氧化物.
充分反应后测得:①A中样品质量为12.0g,②A中剩余固体质量为8.0g,③B装置增重1.8g,④C装置增重2.2g.(各装置均充分吸收,不考虑装置中空气的影响)
(5)B中的试剂是c,C中的试剂是d,D中的试剂是a(填字母序号);
a.碱石灰 b.浓硫酸 c.无水硫酸铜 d.浓NaOH溶液
(6)计算得出样品的组成,只需实验测得四个数据中的三个即可,则可行的组合为abcd(填序号,多选少选不给分).
a.②③④b.①③④c.①②④d.①②③
通过计算可得碱式碳酸铜(aCuCO3•bCu(OH)2•cH2O)中a:b:c=1:1:1.
(7)D的作用防止空气中的二氧化碳进入C中.若将D装置去掉,a值将偏大(填“偏大”、“偏小”或“不变”)
17.量取40ml酒精,应选用的仪器是( )
| A. | 10 ml的量筒 | B. | 100 ml的量筒 | ||
| C. | 50 ml的量筒和胶头滴管 | D. | 500 ml的量筒和胶头滴管 |