题目内容
8.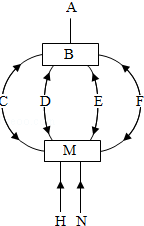 如图为九种物质的相互关系,其中A、B、C、M、N是氧化物,B常温下是液体,C是黑色固体,M、N为气体;H是固体单质,F常温下是固体,D、E中含有三种元素,D能使紫色石蕊溶液变成红色.图中“→”表示转关系“-”表示反应关系(部分反应物、生成物和反应条件未标出).
如图为九种物质的相互关系,其中A、B、C、M、N是氧化物,B常温下是液体,C是黑色固体,M、N为气体;H是固体单质,F常温下是固体,D、E中含有三种元素,D能使紫色石蕊溶液变成红色.图中“→”表示转关系“-”表示反应关系(部分反应物、生成物和反应条件未标出).(1)试写出下列物质的化学式:DH2CO3;FCaCO3;MCO2;
(2)写出以下转化的化学反应方程式:
①A和B的反应:CaO+H2O=Ca(OH)2;该反应会放热.
②E→B的反应:H2SO4+Na2CO3=Na2SO4+H2O+CO2↑;
(3)写出物质M在生活中的一种用途:灭火.
分析 根据A、B、C、M、N是氧化物,B常温下是液体,C是黑色固体,M、N为气体,D、E中含有三种元素,D能使紫色石蕊溶液变成红色,D会转化成B、M,所以B是水,M是二氧化碳,H、N会转化成二氧化碳,所以H是碳,N是一氧化碳,A水与水反应,所以A是氧化钙,C会转化成二氧化碳、水,所以C是氧化铜,F常温下是固体,所以F是碳酸钙,E是硫酸,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、M、N是氧化物,B常温下是液体,C是黑色固体,M、N为气体,D、E中含有三种元素,D能使紫色石蕊溶液变成红色,D会转化成B、M,所以B是水,M是二氧化碳,H、N会转化成二氧化碳,所以H是碳,N是一氧化碳,A水与水反应,所以A是氧化钙,C会转化成二氧化碳、水,所以C是氧化铜,F常温下是固体,所以F是碳酸钙,E是硫酸,经过验证,推导正确,所以D是H2CO3,F是CaCO3,M是CO2;
(2)①A和B的反应是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2,该反应会放热;
②E→B的反应是硫酸和碳酸钠反应生成硫酸钠、水和二氧化碳,化学方程式为:H2SO4+Na2CO3=Na2SO4+H2O+CO2↑;
(3)通过推导可知,M是二氧化碳,可以用来灭火.
故答案为:(1)H2CO3,CaCO3,CO2;
(2)①CaO+H2O=Ca(OH)2,放;
②H2SO4+Na2CO3=Na2SO4+H2O+CO2↑;
(3)灭火.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
7.某+2价金属的氧化物中,金属元素和氧元素的质量比为3:2,该金属元素的相对原子质量为( )
| A. | 24 | B. | 40 | C. | 56 | D. | 64 |
17.如表4个图象,能正确反映对应关系的是( )
| A | B | C | D |
| 向30g稀硫酸中不断滴加15%的Ba(OH)2溶液至过量 | 甲烷和过量的氧气在密闭容器中完全反应 | 同形态等质量的镁粉和铝粉分别与足量的等体积质量分数的稀硫酸反应 | 向一定量PH=2稀硫酸的烧杯中不断加水稀释 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
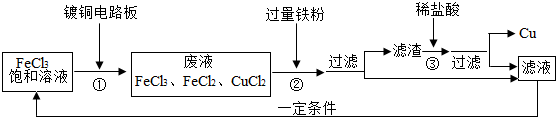
 学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的石灰水、碳酸钠溶液摆放在实验桌上,让同学们区分.下面是“雄鹰小组”同学们的探究过程:
学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的石灰水、碳酸钠溶液摆放在实验桌上,让同学们区分.下面是“雄鹰小组”同学们的探究过程: 实验室利用如图实验装置进行有关化学实验,回答下列问题:
实验室利用如图实验装置进行有关化学实验,回答下列问题: