题目内容
13.有A、B、C、D四种无色溶液,它们可能是盐酸、氢氧化钾、碳酸钠和氢氧化钙四种溶液中的某一种.各取少量,将其两两混合,现象如下:A、B混合,有气泡产生;A、C混合,有白色沉淀产生;其他两两混合,均无明显现象.由此判断四种溶液中的溶质(写化学式):ANa2CO3、BHCl、CCa(OH)2、DKOH.A、C混合时的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.分析 碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠;
氢氧化钾和稀盐酸反应生成氯化钾和水,不能和碳酸钠、氢氧化钙反应.
解答 解:碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠;
氢氧化钾和稀盐酸反应生成氯化钾和水,不能和碳酸钠、氢氧化钙反应,A、B混合,有气泡产生;A、C混合,有白色沉淀产生,说明A是碳酸钠,B是稀盐酸,C是氢氧化钙,因此D是氢氧化钾;
碳酸钠、氯化氢、氢氧化钙、氢氧化钾的化学式分别是Na2CO3、HCl、Ca(OH)2、KOH;
碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
故填:Na2CO3;HCl;Ca(OH)2;KOH;Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
点评 虽然氢氧化钾能和稀盐酸反应生成氯化钾和水,但是无明显现象,要注意理解.

练习册系列答案
相关题目
15.人体缺少下列哪种元素会导致贫血( )
| A. | 碘 | B. | 钙 | C. | 氟 | D. | 铁 |
18.下列化学方程式书写正确的是( )
| A. | 2H2O2$\frac{\underline{\;通电\;}}{\;}$2H2+O2 | B. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$ 2Fe2O3 | ||
| C. | P4+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | D. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O |
3.根据表中内容回答下列问题.
(1)随温度升高,硝酸钾溶解度的变化趋势是增大(填“增大”“减小”或“不变”).
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是大于20℃小于40℃.
(3)取KNO3、NaCl两种固体各36g分别放入20℃时的100g水中充分溶解,20℃时有如图1所示的实验现象,烧杯b中溶解的物质氯化钠.
(4)如图2所示,若向烧杯中加入足量的硝酸铵使之充分溶解,可观察到的现象是烧杯内水温下降,试管中有晶体析出.

(5)如图2所示,若向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是烧杯内浑浊,水温上升,试管内固体逐渐溶解.
| 温度/℃ 溶解度/g 物质 | 0 | 20 | 40 | 60 | 80 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| Ca(OH)2 | 0.173 | 0.165 | 0.121 | 0.116 | 0.094 |
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是大于20℃小于40℃.
(3)取KNO3、NaCl两种固体各36g分别放入20℃时的100g水中充分溶解,20℃时有如图1所示的实验现象,烧杯b中溶解的物质氯化钠.
(4)如图2所示,若向烧杯中加入足量的硝酸铵使之充分溶解,可观察到的现象是烧杯内水温下降,试管中有晶体析出.

(5)如图2所示,若向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是烧杯内浑浊,水温上升,试管内固体逐渐溶解.

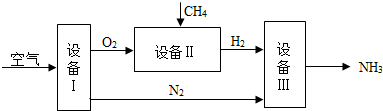
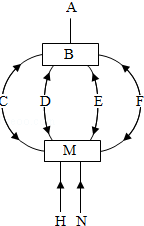 如图为九种物质的相互关系,其中A、B、C、M、N是氧化物,B常温下是液体,C是黑色固体,M、N为气体;H是固体单质,F常温下是固体,D、E中含有三种元素,D能使紫色石蕊溶液变成红色.图中“→”表示转关系“-”表示反应关系(部分反应物、生成物和反应条件未标出).
如图为九种物质的相互关系,其中A、B、C、M、N是氧化物,B常温下是液体,C是黑色固体,M、N为气体;H是固体单质,F常温下是固体,D、E中含有三种元素,D能使紫色石蕊溶液变成红色.图中“→”表示转关系“-”表示反应关系(部分反应物、生成物和反应条件未标出).