题目内容
3.某面包膨松剂由碳酸氢钠(NaHCO3)和碳酸氢铵(NH4HCO3)两种物质组成.某兴趣小组为验证该膨松剂的成分,进行探究,请你参与.[查阅资料]①膨松剂在面包制造过程中发生反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑
②通常状况下,氨气极易溶于水,所得溶液为氨水.
③碱石灰是常用的干燥剂,且可吸收二氧化碳气体.
(1)①中两个化学反应的基本反应类型是分解反应.
[提出问题]面包膨松剂中是否有碳酸氢钠和碳酸氢铵?
[设计实验]设计装置如图所示(实验开始前弹簧夹都处于关闭状态).
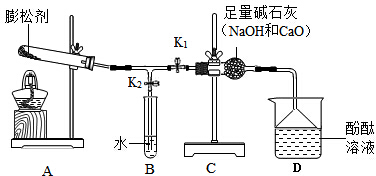
(2)A装置在实验室还可以用于制取氧气气体.
(3)B装置中水的作用是判断反应是否进行完全.
[探究结论](4)利用上述装置进行实验,完成下表内容.
| 实验步骤 | 实验现象 | 实验结论 |
| 膨松剂中有碳酸氢铵 | ||
| 膨松剂中有碳酸氢钠 |
分析 (1)根据①中两个化学反应都是一种反应生成多种物质,属于分解反应进行解答;
(2)根据A装置适用于反应物是固体且需要加热的反应进行解答;
(3)根据水的作用是判断反应是否进行完全,没有气泡说明反应完进行解答;
(4)根据加热碳酸氢铵分解生成氨气、水和二氧化碳,氨气溶于水显碱性,可使酚酞变红;碳酸氢钠分解生成碳酸钠固体和水、二氧化碳进行解答.
解答 解:(1)①中两个化学反应都是一种反应生成多种物质,属于分解反应;故填:分解反应;
(2)A装置适用于反应物是固体且需要加热的反应,所以A装置在实验室还可以用于制取氧气;故填:氧气;
(3)水的作用是判断反应是否进行完全,没有气泡说明反应完;故填:判断反应是否进行完全;
(4)组装好仪器,先检查装置的气密性,如果导管口产生气泡,说明装置不漏气;
装入药品进行加热,打开阀门K1、关闭阀门K2,如果观察到酚酞试液变红色,说明有碳酸氢铵存在;
然后打开阀门K2、关闭阀门K1继续加热,最终观察到B中试管内没有气泡冒出,且原药品中仍有固体残留物,说明有碳酸氢钠存在.
故答案为:
| 实验步骤 | 实验现象 | 实验结论 |
| 装入药品进行加热,打开阀门K1、关闭阀门K2 | 酚酞试液变红 | 膨松剂中有碳酸氢铵 |
| 然后打开阀门K2、关闭阀门K1继续加热 | 最终观察到B中试管内没有气泡冒出,且原药品中仍有固体残留物 | 膨松剂中有碳酸氢钠 |
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
13.将16克硫分别在给定质量的氧气中充分燃烧,其数据如下:
(1)请根据发生化学反应的化学方程式计算第一次反应中的X的值.(写计算过程)
(2)通过计算这三次中三次恰好完全反应?
(3)第二次实验氧气有剩余,剩余2克?
| 第一次 | 第二次 | 第三次 | |
| 氧气的质量 | 10 | 18 | 16 |
| 生成SO2的质量 | X | 32 | 32 |
(2)通过计算这三次中三次恰好完全反应?
(3)第二次实验氧气有剩余,剩余2克?
14.2013年12月2日1时30分,我国成功发射“嫦娥”三号.在航空航天材料中的重要金属钛(Ti)可以用TiO2与Si反应制取,反应的化学方程式为:TiO2+Si═SiO2+Ti,则该反应属于( )
| A. | 分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 复分解反应 |
11.关于溶液的下列说法正确的是( )
| A. | 常温下将100mL饱和Ca(OH)2溶液加热到50℃会变为不饱和溶液 | |
| B. | 从浓度为25%的H2SO4溶液中取出10mL,剩余溶液浓度仍为25% | |
| C. | 20℃时,50克水中溶解了18克NaCl,则20℃时NaCl的溶解度为36克 | |
| D. | 将95克KCl溶液蒸干得到5克固体,则原溶液中KCl的质量分数为5% |
8.已知Si、Al和NaOH溶液反应的化学方程式为:Si+2NaOH+H2O═Na2SiO3+2H2↑;2Al+2NaOH+2H2O═2NaAlO2+3H2↑,Si不与稀盐酸反应.将由硅、铝、铁组成的合金分成两等分,分别于足量的稀盐酸和氢氧化钠溶液充分反应,测得生成氢气的质量相等,则合金中硅、铝、铁的质量比可能是( )
| A. | 28:27:112 | B. | 28:27:56 | C. | 1:2:1 | D. | 1:1:2 |
13.下列物质溶于水,溶液温度明显降低的是( )
| A. | 硝酸铵 | B. | 浓硫酸 | C. | 氢氧化钠 | D. | 氯化钠 |
 下面是教材上的三个实验,请回答问题:
下面是教材上的三个实验,请回答问题: 自热米饭是一种快餐食品.
自热米饭是一种快餐食品.