题目内容
11.关于溶液的下列说法正确的是( )| A. | 常温下将100mL饱和Ca(OH)2溶液加热到50℃会变为不饱和溶液 | |
| B. | 从浓度为25%的H2SO4溶液中取出10mL,剩余溶液浓度仍为25% | |
| C. | 20℃时,50克水中溶解了18克NaCl,则20℃时NaCl的溶解度为36克 | |
| D. | 将95克KCl溶液蒸干得到5克固体,则原溶液中KCl的质量分数为5% |
分析 A、根据氢氧化钙的溶解度随着温度的升高而减小,进行分析判断.
B、根据溶液具有均一性,进行分析判断.
C、溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量.
D、根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%,进行分析判断.
解答 解:A、氢氧化钙的溶解度随着温度的升高而减小,常温下将100mL饱和Ca(OH)2溶液加热到50℃,氢氧化钙的溶解度减小,有1氢氧化钙析出,溶液仍为饱和溶液,故选项错误.
B、溶液具有均一性,从浓度为25%的H2SO4溶液中取出10mL,剩余溶液浓度仍为25%,故选项说法正确.
C、20℃时,50克水中溶解了18克NaCl,没有说明是否达到了饱和状态,则无法确定20℃时NaCl的溶解度,故选项说法错误.
D、将95克KCl溶液蒸干得到5克固体,则原溶液中KCl的质量分数为$\frac{5g}{95g}×$100%>5%,故选项说法错误.
故选:B.
点评 本题难度不大,掌握氢氧化钙的溶解度随着温度的升高而减小、溶液具有均一性、溶解度的概念、溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%是正确解答本题的关键.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
2.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
试推断该密闭容器中发生的化学反应基本类型为分解反应.
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 2 | 2 | 84 | 5 |
| 反应后质量/g | 待测 | 24 | 0 | 14 |
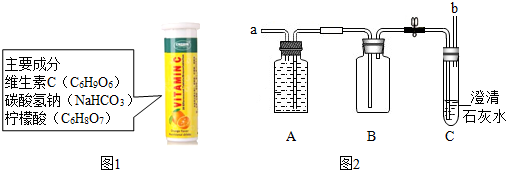
6.某探究小组发现,将维生素C泡腾片(保健药品,其成分见图1)溶于水有许多气体产生,小组同学对产生的气体进行探究.
【提出问题】产生气体的成分是什么?
【猜想假设】
甲间学:该气体可能中CO2、O2、CO、H2、N2的-种或几种.
乙同学:不可能含有N2,因为根据质量守恒定律(或化学反应前后元素种类不变),反应物中不含氮元素.
丙同学:不应含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒.
讨论后大家认为:该气体可能含有CO、O2中的一种或两钟.
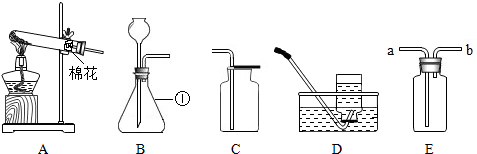
【实验探究】小组同学设计了如图2装置,将气体收集到集气瓶B中进行实验.若要将B中气体排入试管C中,你将采取的方法是从a处吹气.
【探究结论】该气体中一定有二氧化碳.写出实验Ⅰ中发生反应的比学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
【实验拓展】若A中液体为水,进行Ⅰ、Ⅱ实验相同操作,C中也未变浑浊,但b处带火星木条复燃,则得出的结论是该气体为氧气,理由是氧气具有助燃性,能使带火星的木条复燃.

【提出问题】产生气体的成分是什么?
【猜想假设】
甲间学:该气体可能中CO2、O2、CO、H2、N2的-种或几种.
乙同学:不可能含有N2,因为根据质量守恒定律(或化学反应前后元素种类不变),反应物中不含氮元素.
丙同学:不应含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒.
讨论后大家认为:该气体可能含有CO、O2中的一种或两钟.
【实验探究】小组同学设计了如图2装置,将气体收集到集气瓶B中进行实验.若要将B中气体排入试管C中,你将采取的方法是从a处吹气.
| 实验编号 | 实验操作 | 实验现象 |
| Ⅰ | 将A中澄清石灰水排入B中 | B中液体变浑浊,而C中未变浑浊 |
| Ⅱ | 将带火星的木条靠近b处 | 带火星的木条没有复燃 |
【实验拓展】若A中液体为水,进行Ⅰ、Ⅱ实验相同操作,C中也未变浑浊,但b处带火星木条复燃,则得出的结论是该气体为氧气,理由是氧气具有助燃性,能使带火星的木条复燃.
 如图是测定空气中氧气含量试验的改进装置.
如图是测定空气中氧气含量试验的改进装置.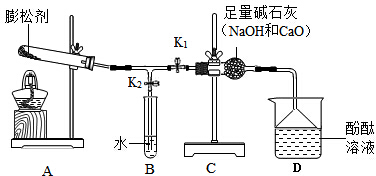
 已知:A、B、C、D是中学化学常见的物质,其中A、C为化合物,B、D为单质,它们之间能够发生如下反应:
已知:A、B、C、D是中学化学常见的物质,其中A、C为化合物,B、D为单质,它们之间能够发生如下反应: