题目内容
8.已知Si、Al和NaOH溶液反应的化学方程式为:Si+2NaOH+H2O═Na2SiO3+2H2↑;2Al+2NaOH+2H2O═2NaAlO2+3H2↑,Si不与稀盐酸反应.将由硅、铝、铁组成的合金分成两等分,分别于足量的稀盐酸和氢氧化钠溶液充分反应,测得生成氢气的质量相等,则合金中硅、铝、铁的质量比可能是( )| A. | 28:27:112 | B. | 28:27:56 | C. | 1:2:1 | D. | 1:1:2 |
分析 根据铝跟盐酸或氢氧化钠溶液都能发生反应,而铁只与稀盐酸反应生成氢气,硅与氢氧化钠溶液反应生成氢气;利用反应的化学方程式确定铝与氢气的质量关系,进而进行分析判断即可.
解答 解:根据题目信息可知,铁和铝与稀盐酸生成氢气,铝和硅与氢氧化钠生成氢气.铝和盐酸的反应方程式:2Al+6HCl=2AlCl3+3H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,说明相同质量的铝与盐酸或者氢氧化钠生成氢气的质量相等.综合分析,铁和盐酸生成的氢气的质量等于硅和氢氧化钠生成的氢气的质量.设铁与盐酸生成的氢气的质量为M,则硅的质量为X,铁的质量为Y.
Si+2NaOH+H2O═Na2SiO3+2H2↑
28 4
X M
则$\frac{28}{4}=\frac{X}{M}$,解得:X=7M
Fe+2HCl=FeCl2+H2↑
56 2
Y M
则$\frac{56}{2}=\frac{Y}{M}$,解得:Y=28M
∴合金中硅和铁的质量之比=7M:28M=1:4.
故选A.
点评 本题需要掌握化学方程式的计算格式和规范性,注意:相同质量的铝与盐酸或者氢氧化钠生成氢气的质量相等.

练习册系列答案
相关题目
18.某同学从定量角度研究双氧水制取氧气的过程,对原实验进行部分改进,增加了称量操作.具体做法是:取10%的双氧水和少量的二氧化锰放入气体发生装置,并对反应前后混合物的质量进行称量,记录如下:
若反应后,双氧水分解完全且氧气全部逸出,该同学得出的结论中,不合理的是( )
| 反应过程 | 反应前 | 反应后 |
| 质量变化(不含容器质量) | 34.3g | 32.7g |
| A. | 该化学反应前后分子总数不变 | B. | 最多得到氧气的质量为1.6g | ||
| C. | 催化剂二氧化锰的质量为0.3g | D. | 反应得到水和氧气的质量比为9:8 |
17.下列实验结论错误的是( )
| 选项 | A | B | C | D |
| 实 验 |  |  |  |  |
| 实验 现象 | 热水中未燃烧的白磷在通入氧气后燃烧 | 带火星的木条伸入氧气中复燃 | 紫色石蕊试液在通入二氧化碳后变化 | 燃烧的蜡烛由低到高依次熄灭 |
| 实验 结论 | 燃烧需要氧气 | 氧气浓度越大,燃烧越剧烈 | 使石蕊变红的是二氧化碳 | 二氧化碳密度比空气大 |
 如图是测定空气中氧气含量试验的改进装置.
如图是测定空气中氧气含量试验的改进装置.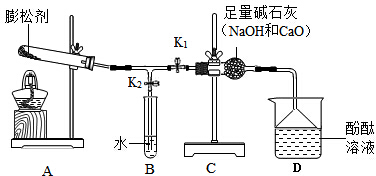

 如图表示一瓶硫酸锌溶液,请填写下列空白.
如图表示一瓶硫酸锌溶液,请填写下列空白.