题目内容
12. 如图是初中化学中非常重要的装置.
如图是初中化学中非常重要的装置. 同学们利用如图做了如下实验(A、B、C中盛放有不同的药品):
友情提示:2FeCl3+Fe→3FeCl2
【实验1】若B中为生锈的铁片,打开K1、K2,将A中稀盐酸加入B中,关闭K1,观察到C中有气泡冒出,反应过程中B中出现的现象为溶液逐渐由棕黄色变为浅绿色,生锈的铁片逐渐减少;B中铁锈与稀盐酸反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O,Fe+2HCl=FeCl2+H2↑;反应后B中的溶质一定含有FeCl2.
【实验2】若B中集满二氧化碳气体,A为氢氧化钠溶液,C中为氢氧化钙溶液,则利用此装置可以证明二氧化碳能与氢氧化钠发生化学反应,操作为打开K1,将A中氢氧化钠加入B中,关闭K1,打开K2,观察到现象为C中氢氧化钙溶液无变化,C中水会倒流进入B瓶.
分析 【实验1】根据除铁锈和铁防锈的知识就能得出本题的正确答案;
【实验2】打开K1,将A中氢氧化钠加入B中,关闭K1,打开K2,根据压强的变化,推测现象.
解答 解:【实验1】根据氧化铁与稀盐酸反应生成氯化铁和水,该反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O,而2FeCl3+Fe=3FeCl2,Fe+2HCl=FeCl2+H2↑;
【实验2】若B中集满二氧化碳气体,A为氢氧化钠溶液,C中为氢氧化钙溶液,则利用此装置可以证明二氧化碳能与氢氧化钠发生化学反应,操作为打开K1,将A中氢氧化钠加入B中,关闭K1,打开K2,观察到现象为C中氢氧化钙溶液无变化,C中水会倒流进入B瓶.
故答案为:
【实验1】溶液逐渐由棕黄色变为浅绿色,生锈的铁片逐渐减少; Fe2O3+6HCl=2FeCl3+3H2O,Fe+2HCl=FeCl2+H2↑; FeCl2.
【实验2】打开K1,将A中氢氧化钠加入B中,关闭K1,打开K2,C中氢氧化钙溶液无变化,C中水会倒流进入B瓶.
点评 本题主要考查化学方程式的书写方法、除铁锈、铁防锈等方面的知识和基本反应类型的判断,难度稍大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.海藻中含有丰富的碘,实验室从海藻中提取碘单质的反应方程式为:2NaI+Cl2=2NaCl+I2,该反应的基本类型属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
3.下列实验操作中,正确的是( )
| A. |  点燃酒精灯 点燃酒精灯 | B. |  | C. |  液体加热 液体加热 | D. |  |
20.食用豆腐能使人体获得所需要的多种氨基酸,其中含量最多的是亮氨酸(化学式:C6H13NO2),下列有关亮氨酸的说法中,正确的是( )
| A. | 亮氨酸中的含氮量约为10.7% | |
| B. | 亮氨酸中碳、氢元素的质量比为6:13 | |
| C. | 亮氨酸由22个原子构成 | |
| D. | 亮氨酸的分子中含有一个氧分子 |
7.下列除去杂质的方法中,正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | 稀盐酸 | 氯化钠 | 加入适量的氢氧化钠溶液 |
| B | 铜粉 | 铁粉 | 加入足量的稀盐酸溶解、过滤、洗涤 |
| C | 二氧化碳 | 一氧化碳 | 点燃 |
| D | 氯化铁溶液 | 氯化铜 | 加入过量铁粉、过滤 |
| A. | A | B. | B | C. | C | D. | D |
17.以下是一个化学反应的微观示意图.从该示意图中获取的信息正确的是( )


| A. | 反应前后元素种类发生改变 | |
| B. | 该反应的基本类型是化合反应 | |
| C. | 反应前后分子种类不发生改变 | |
| D. | 参加反应的两种分子的个数比是1:2 |
4.某同学为了除去炭粉中混有的少量氧化铜而得到纯净的炭粉,设计了如下方案:①直接将混合物高温加热;②加入稀硫酸并微热后过滤、干燥;③通入(CO并加热;④在CO2气流中高温灼烧.正确的是( )
| A. | ①④ | B. | ②③ | C. | ② | D. | ④ |
1.实验室中的许多药品需要密封保存,下列物质暴露在空气中会变质的是( )
| A. | 氯化钠 | B. | 浓硫酸 | C. | 浓盐酸 | D. | 熟石灰 |
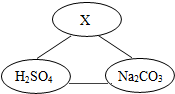 如图所示,各连线两端物质相互都能发生反应,试推断X可能是C
如图所示,各连线两端物质相互都能发生反应,试推断X可能是C