题目内容
17.金属在生产生活中应用广泛.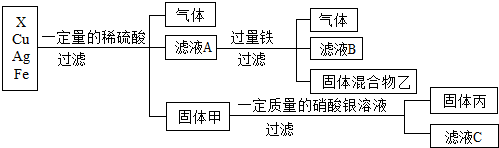
(1)铁制品容易锈蚀,预防铁制品生锈的措施有刷漆(写1条即可).
(2)“湿法炼铜”的原理是铁与硫酸铜溶液反应,该反应的化学方程式是Fe+CuSO4=FeSO4+Cu.
(3)用一氧化碳和赤铁矿(主要成分Fe2O3)炼铁的化学方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)某同学对X、银、铜、铁四种金属混合物的成分进行探究,流程如图所示:
①四重金属的活动性由强到弱的顺序是Fe>X>Cu>Ag.
②固体丙的组成可能是铜、银或银.
分析 根据已有的金属的锈蚀因素、金属与盐溶液的反应、一氧化碳还原氧化铁以及金属活动性顺序的意义进行分析解答即可.
解答 解:(1)铁制品容易锈蚀,预防铁制品生锈的措施有刷漆、涂油等,故填:刷漆;
(2)“湿法炼铜”的原理是铁与硫酸铜溶液反应,该反应的化学方程式是Fe+CuSO4=FeSO4+Cu,故填:Fe+CuSO4=FeSO4+Cu.
(3)用一氧化碳和赤铁矿(主要成分Fe2O3)炼铁,生成的是铁和二氧化碳,反应的化学方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)根据金属的活泼性顺序:铁>氢>铜>银,所以向铁、X、铜、银的金属混合物中加入稀硫酸,铁一定参加反应产生气泡,而铜和银一定没反应,得到的滤液A再加入过量的铁得到混合物乙和滤液B,说明铁除了和过量的硫酸反应产生气体外,还和盐溶液发生了置换反应,因此说明铁的活动性比X强,且X位于氢前;由于硫酸过量,固体甲含有铜和银,铜和硝酸银反应产生硝酸铜和银,因此:
①四种金属的活动性顺序由强到弱的是Fe>X>Cu>Ag;故填:Fe>X>Cu>Ag;
②固体丙的组成可能是:铜、银或银.故填:铜、银或银.
点评 本题以实验设计流程的形式让学生去利用金属活动性顺序表解决有关金属化学性质的问题,有一定的难度,解题的关键是熟练运用金属活动性的顺序意义和掌握金属锈蚀的条件.

练习册系列答案
相关题目
7.根据你的生活经验和所学的化学知识,判断下列做法能达到目的是( )
| A. | 煤炉火上放一盆水,就能防止一氧化碳中毒 | |
| B. | 用生石灰固体来除去二氧化碳中的水蒸气 | |
| C. | 用燃烧的小木条放入集气瓶内来检验二氧化碳是否集满 | |
| D. | 用灼烧闻气味的方法区分羊毛线和棉线 |
12.下列实验现象描述与事实不符合的是( )
| A. | 镁与稀盐酸反应产生气体,放出热量 | |
| B. | 木炭在氧气中燃烧,发出白光,有固体生成 | |
| C. | 水通电一段时间后,电源正极与负极产生的气体体积比约为1:2 | |
| D. | 将铁钉放在硫酸铜溶液中,铁钉上有红色固体附着,一段时间后,蓝色溶液逐渐变为黄色 |
 金属与金属矿物
金属与金属矿物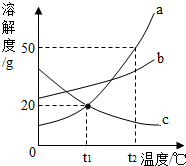 如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题:
如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题: A、B、C、D、E、F为初中化学常见的物质,它们之间的关系如下图所示(“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质.反应条件、部分反应物和生成物已略去).其中A由一种元素组成,B、C是由两种元素组成的不同类别的物质,D、E、F是由三种元素组成的不同类别的物质,且A、B、D含有一种相同的元素,D、E、F也含有一种相同的元素.
A、B、C、D、E、F为初中化学常见的物质,它们之间的关系如下图所示(“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质.反应条件、部分反应物和生成物已略去).其中A由一种元素组成,B、C是由两种元素组成的不同类别的物质,D、E、F是由三种元素组成的不同类别的物质,且A、B、D含有一种相同的元素,D、E、F也含有一种相同的元素.