题目内容
19.完成下列反应的化学方程式,并回答有关问题.(1)绿色植物的光合作用:6CO2+6H2O$\frac{\underline{\;\;\;\;\;光\;\;\;\;\;}}{叶绿体}$C6H12O6+6O2,该反应中的能量转化是太阳能转化为化学能.
(2)用一氧化碳还原磁铁矿炼铁4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
(3)证明铜的金属活动性比银强Cu+2AgNO3=Cu(NO3)2+2Ag.
(4)硫酸与氢氧化钡溶液混合H2SO4+Ba(OH)2═BaSO4↓+2H2O,反应的实质是H+与OH-结合生成H2O、Ba2+与SO42-结合生成BaSO4沉淀,故溶液导电性减弱.
(5)氢氧化亚铁与空气中的氧气、水发生反应生成氢氧化铁4Fe(OH)2+2H2O+O2=4Fe(OH)3.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)绿色植物的光合作用的方程式为:6CO2+6H2O$\frac{\underline{\;\;\;\;\;光\;\;\;\;\;}}{叶绿体}$C6H12O6+6O2;在该反应中太阳能转化为化学能;
(2)磁铁矿的主要成分是四氧化三铁,一氧化碳与四氧化三铁反应生成铁和二氧化碳,反应的化学方程式为:4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;
(3)根据金属活动顺序表可知,铜把银盐中的银置换出来可证明铜的金属活动性比银强,反应的化学方程式为:Cu+2AgNO3=Cu(NO3)2+2Ag;
(4)硫酸与氢氧化钡溶液混合生成硫酸钡沉淀和水,反应的化学方程式为:H2SO4+Ba(OH)2═BaSO4↓+2H2O;反应的实质是H+与OH-结合生成H2O,
Ba2+与SO42-结合生成BaSO4沉淀.
(5)氢氧化亚铁与空气中的氧气、水发生反应生成氢氧化铁,反应的化学方程式为:4Fe(OH)2+2H2O+O2=4Fe(OH)3;
故答案为:(1)6CO2+6H2O$\frac{\underline{\;\;\;\;\;光\;\;\;\;\;}}{叶绿体}$C6H12O6+6O2;太阳能转化为化学能
(2)4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 (3)Cu+2AgNO3=Cu(NO3)2+2Ag
(4)H2SO4+Ba(OH)2═BaSO4↓+2H2O;
H+与OH-结合生成H2O沉淀,Ba2+与SO42-结合生成BaSO4沉淀
(5)4Fe(OH)2+2H2O+O2=4Fe(OH)3
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

| A. | 硫在氧气中燃烧发出蓝紫色火焰,因此物质燃烧均能看到火焰 | |
| B. | 能使无色酚酞溶液变红色的溶液一定显碱性,但不一定是碱溶液 | |
| C. | 可以给人类供能的营养物质有糖类、油脂和无机盐 | |
| D. | 含有相同的核电荷数的粒子一定属于同种元素 |
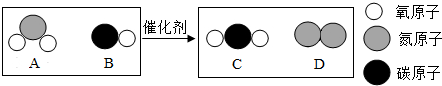
对此反应的叙述不正确的是( )
| A. | 反应前后分子数目未发生改变 | |
| B. | 利用此反应可减少有毒气体的排放 | |
| C. | 该反应中B与D的质量比为4:1 | |
| D. | 该反应中A与B的化学计量数之比为1:2 |
| A. | 金刚石 | B. | 蛋白质 | C. | 氯化钠 | D. | 液态水 |
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3/g | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl/g | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
(2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为163.9g.
(3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过降温结晶方法获得较纯净的KNO3晶体.
(4)根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是36g~36.3g.
(5)某温度下,将一定质量的KNO3溶液进行恒温蒸发结晶,实验过程如图所示,则是蒸发前原溶液是不饱和(填“饱和”或“不饱和”)溶液.n的数值是9.

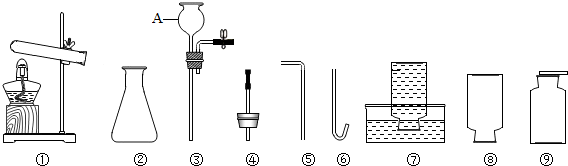
(1)图中仪器名称是②锥形瓶,⑧集气瓶.
(2)小宝同学用氯酸钾和二氧化锰制取并收集一瓶氧气,应选择上图中的仪器①④⑤⑨(或①④⑥⑦)(填序号,以下同),其化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;验证瓶中氧气已集满的方法是将带火星的木条放到瓶口,如果木条复燃,则已收满.
(3)小茹同学用锌和稀硫酸制取H2,同时生成硫酸锌,则应选择上图中②③⑥⑦装置,其化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
(4)小佳同学查阅资料得到制取硫化氢气体的如下信息,请回答下列问题:
| 气体 | 实验药品 | 反应条件 | 气体物理性质 |
| H2S | 硫化亚铁固体与稀硫酸 | 不需加热 | 无色,密度比空气大,可溶于水 |
②制取硫化氢可以(填“可以”或“不可以”)采用装置②和③,理由是反应物是固体和液体,且反应不需要加热.
 某“管道疏通剂”(部分说明如图),其原理是利用铝与氢氧化钠溶液反应时放出大量的热,以加快氢氧化钠与毛发等淤积物的作用,反应的原理为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
某“管道疏通剂”(部分说明如图),其原理是利用铝与氢氧化钠溶液反应时放出大量的热,以加快氢氧化钠与毛发等淤积物的作用,反应的原理为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.