题目内容
13. 化学兴趣小组的同学在实验室整理存放盐溶液的药品柜时,发现有一瓶标签受到腐蚀的无色溶液,如图所示.
化学兴趣小组的同学在实验室整理存放盐溶液的药品柜时,发现有一瓶标签受到腐蚀的无色溶液,如图所示.【提出问题】这瓶无色溶液究竟是什么溶液?
【猜想与假设】该无色溶液可能是氯化钠、碳酸钠、碳酸氢钠、硫酸钠中某一种的溶液.
【初步分析】
(1)小红同学根据标签上的组成元素认为一定不是氯化钠溶液.
(2)小明同学提出,溶液也不可能是碳酸氢钠,他的依据是碳酸氢钠的化学式中钠元素右下角的数字为1.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
| 实验操作 | 实验现象 |
| 取少重该无色溶液于试管中,滴加稀盐酸 | 产生大量气泡. |
(3)该瓶无色溶液的溶质是Na2CO3(填化学式).生成气体的化学反应方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
【实验反思】
(4)你认为选用其它类别的哪种物质,同样可以达到鉴别剩余两种盐的目的.写出实验操作步骤及实验现象:取待测液涂在pH试纸上,pH大于7,则该溶液是碳酸钠溶液
(5)实验结束后,他们向同学们提出了如下建议:
①要有严谨的科学实验的态度 ②倾倒液体时应注意保护标签不被腐蚀 ③无法辨认的药品,无需保留,直接倒掉.
你认为合理的是①②(填序号).
分析 根根据题干提供的信息进行分析,残缺的标签中钠元素的右下角有数字2,且含有氧元素,故不可能是氯化钠、碳酸氢钠和硝酸钠,可以据此完成(1)(2)两小题;
[实验结论]硫酸钠溶液和碳酸钠溶液都能与氯化钡溶液反应生成白色沉淀,但是碳酸钡沉淀能和盐酸反应产生气体,而硫酸钡不能溶于稀盐酸,可以据此完成解答;
(3)根据碳酸盐能与盐酸反应生成二氧化碳气体,据此解答即可;
(4)根据碳酸钠溶液呈碱性,硫酸钠溶液呈中性解答;
(5)根据药品的使用以及注意事项进行分析解答.
解答 解:(1)氯化钠是由钠元素和氯元素组成的,不含有氧元素,故一定不会是氯化钠溶液,故填:氯化钠;
(2)此标签中钠元素右下角的数字为2,而碳酸氢钠的化学式为NaHCO3,故不会是碳酸氢钠,故填:碳酸氢钠;碳酸氢钠的化学式中钠元素右下角的数字为1;
(3)碳酸钠能与盐酸反应产生二氧化碳气体,因为加入盐酸产生气体,故该物质是碳酸钠,故填:Na2CO3;Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(4)碳酸钠溶液呈碱性,硫酸钠溶液呈中性,故可以使用pH试纸测定溶液的pH;故填:取待测液涂在pH试纸上,pH大于7,则该溶液是碳酸钠溶液;
(5)①要有严谨的科学实验的态度,正确;
②倾倒液体时应注意保护标签不被腐蚀,正确;
③无法辨认的药品,无需保留,直接倒掉,错误;
故填:①②.
点评 本题考查了破损标签瓶中试剂的确定,完成此题,可以依据破损标签中所含有的元素以及有关物质的性质进行分析及设计实验.

练习册系列答案
相关题目
3.为了探究某稀盐酸的质量分数,甲乙同学分别取了等质量的稀盐酸100g,甲同学加入8g氧化铜,反应后固体全部消失;乙同学加入16g氧化铜,反应后有固体剩余,下列推断正确的是( )
| A. | 反应后甲同学所得溶液中加入少量氢氧化钠溶液,一定有蓝色沉淀 | |
| B. | 反应后乙同学所得溶液中一定不含盐酸 | |
| C. | 反应后甲乙同学所得溶液的溶质质量分数一样 | |
| D. | 原稀盐酸中质量分数一定大于7.3%小于14.6% |
8.下列实验一定达到实验目的是( )
| A. | Na2CO3、K2SO4、BaCl2、HCI四种溶液不需另加试剂既能鉴别 | |
| B. | 用点燃后在火焰上方罩一个干冷烧杯的方法来鉴别H2和CH4 | |
| C. | 进入了少量空气的玻璃管来做托里拆利实验 | |
| D. | 通过增减在海绵上面的砖上的砝码,观察海绵凹陷情况,探究力的作用效果与受力面积的关系 |
18.在过氧化氢制氧气的化学变化的过程中,最小的粒子是( )
| A. | H2O2 | B. | H2O | C. | O2 | D. | H和O |
2.下列叙述不正确的是( )
| A. | 不能用铁制容器盛装农药波尔多液 | |
| B. | 人体胃液的pH在0.9-1.5之间 | |
| C. | 用炉具清洁剂可以去除水壶中的水垢 | |
| D. | 蚊虫叮咬后涂抹牙膏或肥皂水止痒 |
3.一氧化碳与氢气在一定条件下发生反应的化学方程式是2CO+4H2 $\frac{\underline{\;一定条件\;}}{\;}$ X+H2O.下列分析正确的是( )
| A. | X中只含C、H元素 | B. | X与CO的相对分子质量之差为16 | ||
| C. | 该反应的基本类型是置换反应 | D. | X中C、H元素质量比为4:1 |
 (1)取一只蜡烛,认真观察,并且下一小块,放入水中,蜡烛浮在水面,结论:石蜡的颜色为白色,状态为固体,密度比水小.
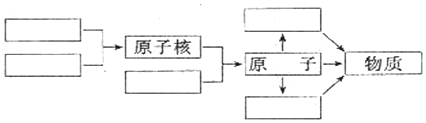
(1)取一只蜡烛,认真观察,并且下一小块,放入水中,蜡烛浮在水面,结论:石蜡的颜色为白色,状态为固体,密度比水小.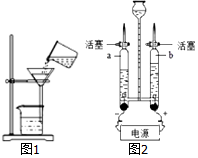 海水是一种化学成分复杂的混合物,除了水还包括溶解于水中的丰富的矿物质和少量气体.
海水是一种化学成分复杂的混合物,除了水还包括溶解于水中的丰富的矿物质和少量气体.