题目内容
3.为了探究某稀盐酸的质量分数,甲乙同学分别取了等质量的稀盐酸100g,甲同学加入8g氧化铜,反应后固体全部消失;乙同学加入16g氧化铜,反应后有固体剩余,下列推断正确的是( )| A. | 反应后甲同学所得溶液中加入少量氢氧化钠溶液,一定有蓝色沉淀 | |
| B. | 反应后乙同学所得溶液中一定不含盐酸 | |
| C. | 反应后甲乙同学所得溶液的溶质质量分数一样 | |
| D. | 原稀盐酸中质量分数一定大于7.3%小于14.6% |
分析 A、根据酸、碱、盐、氧化物之间发生反应的条件进行分析.
B、反应结束,或者是盐酸反应完,或者是氧化铜反应完,或者是盐酸和氧化铜都反应完,不可能盐酸和氧化铜都有剩余.
C、若二者反应物的质量一样,则所得溶液中溶质的质量分数相等.
D、甲可能恰好完全反应,也可能盐酸过量,乙盐酸一定反应完,根据此三种情况分别算出稀盐酸中溶质的质量分数.
解答 解:A、氧化铜与盐酸反应生成了氯化铜,氢氧化钠与氯化铜反应会生成蓝色的氢氧化铜沉淀,而甲反应结束后氧化铜反应完,还可能有剩余的盐酸,若有剩余盐酸,盐酸又会与氢氧化铜反应生成氯化铜和水,不会出现蓝色沉淀.故错误;
B、乙反应结束后,固体有剩余,也就是氧化铜有剩余,那么盐酸一定反应完.故正确;
C、若8g氧化铜与100g稀盐酸恰好完全反应,则甲恰好完全反应,乙会剩余8g氧化铜,此种情况下,反应后甲、乙两同学所得的溶液中溶质的质量分数相等.但题中没有说明甲乙反应的具体质量关系,因此不能判断反应后溶质的质量分数关系,故错误;
D、甲若恰好完全反应,依据化学方程式中氧化铜的质量计算可计算得稀盐酸中溶质的质量分数为7.3%,而不是大于7.3%.故错误.
故选B.
点评 本题难度较大,主要考查了金属和酸的反应,并根据有关的反应进行相关的计算,培养学生的分析问题、解决问题的能力.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
13.下列关于“一定”的说法一定正确的是( )
| A. | 电离时不出现氢氧根离子的物质一定不呈碱性 | |
| B. | 金属活动性靠前的物质一定能将靠后的物质从它的溶液中置换出来 | |
| C. | 做功的过程中,一定实现能量的转化 | |
| D. | 酵母菌一定要在无氧环境中才能存活 |
14.根据如图的信息判断,下列关于铝的说法错误的是( )
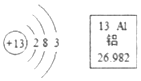

| A. | 属于金属元素 | |
| B. | 相对原子质量是26.982g | |
| C. | 铝元素在化合物中显正价 | |
| D. | 在化学反应中,原子易失去电子形成Al3+ |
18.下列用化学知识来分析生活、生产中的问题,正确的是( )
| A. | 高层住房着火时,立即打开所有门窗 | |
| B. | 用一种高效的催化剂可把水变成汽油 | |
| C. | 蚊虫叮咬后,会在人的皮肤内分泌蚁酸使皮肤肿痛,可涂点小苏打来减轻痛痒 | |
| D. | 用淀粉溶液检验食盐中是否含碘 |
8.某有机物R完全燃烧的化学方程式为:R+O2═CO2+H2O(方程式已配平),则关于R组成的说法中,正确的是
①只含有C、H两元素 ②一定含有C、H两元素,可能含有O元素 ③一定含有C、H、O三种元素 ④C、H元素的质量比为3:1 ⑤C、H、O元素的质量比为6:1:8( )
①只含有C、H两元素 ②一定含有C、H两元素,可能含有O元素 ③一定含有C、H、O三种元素 ④C、H元素的质量比为3:1 ⑤C、H、O元素的质量比为6:1:8( )
| A. | 只有① | B. | 只有② | C. | 有①④ | D. | 有③⑤ |
12.分类、归纳、比较、思考、合作都是经常用到的学习方法.请回答:
(1)化学是一门以实验为基础的科学,一个学期以来,我们接触了很多实验:
请从实验中体现物质性质的角度,将上述实验平均分为两类,其中的一个分类标准
是①体现物质化学性质的实验[或体现物质物理性质的实验],包括实验为②A、C[或B、D](填字母).
(2)在元素周期表中与氯元素同族的元素还有氟和第四周期的溴以及第五周期的碘等.氟气、溴、碘的三种单质的化学性质与氯气相似,都具有氧化性,已知四种单质的氧化性随元素原子的核电荷数的增大而逐渐减弱.据此可以判断四种单质中氧化性最弱的是碘(写名称).
(1)化学是一门以实验为基础的科学,一个学期以来,我们接触了很多实验:
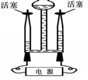 | 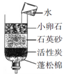 | 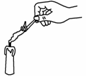 |  |
| A.通电使水分解 | B.自制简易净水器 | C.点燃蜡烛熄灭 后产生的白烟 | D.200g水露置在空气 中一段时间后变成175g |
是①体现物质化学性质的实验[或体现物质物理性质的实验],包括实验为②A、C[或B、D](填字母).
(2)在元素周期表中与氯元素同族的元素还有氟和第四周期的溴以及第五周期的碘等.氟气、溴、碘的三种单质的化学性质与氯气相似,都具有氧化性,已知四种单质的氧化性随元素原子的核电荷数的增大而逐渐减弱.据此可以判断四种单质中氧化性最弱的是碘(写名称).
13. 化学兴趣小组的同学在实验室整理存放盐溶液的药品柜时,发现有一瓶标签受到腐蚀的无色溶液,如图所示.
化学兴趣小组的同学在实验室整理存放盐溶液的药品柜时,发现有一瓶标签受到腐蚀的无色溶液,如图所示.
【提出问题】这瓶无色溶液究竟是什么溶液?
【猜想与假设】该无色溶液可能是氯化钠、碳酸钠、碳酸氢钠、硫酸钠中某一种的溶液.
【初步分析】
(1)小红同学根据标签上的组成元素认为一定不是氯化钠溶液.
(2)小明同学提出,溶液也不可能是碳酸氢钠,他的依据是碳酸氢钠的化学式中钠元素右下角的数字为1.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
【实验结论】
(3)该瓶无色溶液的溶质是Na2CO3(填化学式).生成气体的化学反应方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
【实验反思】
(4)你认为选用其它类别的哪种物质,同样可以达到鉴别剩余两种盐的目的.写出实验操作步骤及实验现象:取待测液涂在pH试纸上,pH大于7,则该溶液是碳酸钠溶液
(5)实验结束后,他们向同学们提出了如下建议:
①要有严谨的科学实验的态度 ②倾倒液体时应注意保护标签不被腐蚀 ③无法辨认的药品,无需保留,直接倒掉.
你认为合理的是①②(填序号).
 化学兴趣小组的同学在实验室整理存放盐溶液的药品柜时,发现有一瓶标签受到腐蚀的无色溶液,如图所示.
化学兴趣小组的同学在实验室整理存放盐溶液的药品柜时,发现有一瓶标签受到腐蚀的无色溶液,如图所示.【提出问题】这瓶无色溶液究竟是什么溶液?
【猜想与假设】该无色溶液可能是氯化钠、碳酸钠、碳酸氢钠、硫酸钠中某一种的溶液.
【初步分析】
(1)小红同学根据标签上的组成元素认为一定不是氯化钠溶液.
(2)小明同学提出,溶液也不可能是碳酸氢钠,他的依据是碳酸氢钠的化学式中钠元素右下角的数字为1.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
| 实验操作 | 实验现象 |
| 取少重该无色溶液于试管中,滴加稀盐酸 | 产生大量气泡. |
(3)该瓶无色溶液的溶质是Na2CO3(填化学式).生成气体的化学反应方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
【实验反思】
(4)你认为选用其它类别的哪种物质,同样可以达到鉴别剩余两种盐的目的.写出实验操作步骤及实验现象:取待测液涂在pH试纸上,pH大于7,则该溶液是碳酸钠溶液
(5)实验结束后,他们向同学们提出了如下建议:
①要有严谨的科学实验的态度 ②倾倒液体时应注意保护标签不被腐蚀 ③无法辨认的药品,无需保留,直接倒掉.
你认为合理的是①②(填序号).
 电动剃须刀因为其方便耐用而被广泛使用,剃须刀的刀头是关键,现在比较好的剃须刀都是水洗刀头,也就是说这种剃须刀的刀头虽然是金属制造的,但是却可以用水直接冲洗.冲洗完晾干就可以了,这说明到刀头上的金属材料必须具备(1)B化学性质;
电动剃须刀因为其方便耐用而被广泛使用,剃须刀的刀头是关键,现在比较好的剃须刀都是水洗刀头,也就是说这种剃须刀的刀头虽然是金属制造的,但是却可以用水直接冲洗.冲洗完晾干就可以了,这说明到刀头上的金属材料必须具备(1)B化学性质;