题目内容
3.镁是一种化学性质较活泼的金属,在空气中表面易氧化.取镁条3g置于烧杯中,加入稀硫酸至不再产生气泡,用去稀硫酸30g,烧杯中剩余物的总质量为32.8g(不考虑其他因素影响).求该镁条中金属镁的质量分数.分析 氧化镁和稀硫酸反应生成硫酸镁和水,镁和稀硫酸反应生成硫酸镁和氢气,反应前后的质量差即为反应生成氢气的质量,根据氢气的质量可以计算镁的质量,进一步可以计算该镁条中金属镁的质量分数.
解答 解:设镁的质量为x,
反应生成氢气的质量为:3g+30g-32.8g=0.2g,
Mg+H2SO4═MgSO4+H2↑,
24 2
x 0.2g
$\frac{24}{x}$=$\frac{2}{0.2g}$,
x=2.4g,
该镁条中金属镁的质量分数为:$\frac{2.4g}{3g}$×100%=80%,
答:该镁条中金属镁的质量分数为80%.
点评 因为只有镁和稀硫酸反应生成氢气,因此反应前后的质量差就是反应生成氢气的质量,这是解答的关键,要注意理解.

练习册系列答案
相关题目
14.下列做法错误的是( )
| A. | 用食盐腌渍菜、鱼、肉、蛋的方法可以延长食物的保存时间 | |
| B. | 用洗涤剂乳化油脂的方法除去餐具上的油污 | |
| C. | 用喷漆的方法防止自行车链条锈蚀 | |
| D. | 用沉淀、过滤、吸附等净化方法,可以使浑浊的水变澄清 |
11.在探究盐酸和氢氧化钙能否发生化学反应时,设计了如下表所示的对照实验.阅读实验内容,并将步骤2中的实验现象填写完整:
为了使对比实验结论可靠,必须保证上述步骤1中加入水的质量以及步骤2中加入含等量水的浓盐酸的用量相同,这个实验中,溶液里明显减少的粒子是OH-和H+(写符号).针对小明氢氧化钙难溶于水的错误结论,请你帮他补充实验证明氢氧化钙微溶于水在一定量的氢氧化钙粉末中加入适量的水,再滴加2∽3滴酚酞试液,浑浊液变红,说明氢氧化钙的溶解性是微溶于水.
| 实验步骤 | 实验现象 | 实验结论 |
| 1.用药匙尾端挑一点氢氧化钙粉末,分别加入A、B两支试管中,各加1mL水振荡 | 两试管中液体均呈白色浑浊状态 | 不填 |
| 2.在A试管中再加少量水振荡试管;向B试管中加入少量浓盐酸,振荡试管 | A试管中液体仍然呈白色浑浊状态.B试管中 白色浑浊消失成为无色溶液 | 氢氧化钙难溶于水;氢氧化钙能与盐酸反应生成易溶物质 |
5.对知识的归纳是学习化学的一种重要方法,下列归纳正确的是( )
| A. | 汽油和洗涤剂除油污的原理相同 | |
| B. | 空气、糖水、高锰酸钾都属于混合物 | |
| C. | 纯碱、烧碱都属于碱 | |
| D. | 只有当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生 |
3.人类已能操纵原子制造分子,若用该方法制造葡萄糖(C6H12O6),不需要的原子是( )
| A. | 氮原子 | B. | 氧原子 | C. | 氢原子 | D. | 碳原子 |
 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则: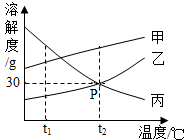 甲、乙、丙三种物质的溶解度曲线如图所示,请根据图回答下列有关问题:
甲、乙、丙三种物质的溶解度曲线如图所示,请根据图回答下列有关问题: