题目内容
以黄铁矿为原料(主要成分是FeS2),生产硫酸的简要流程图如图: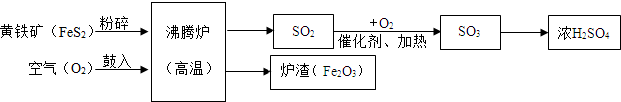
(1)流程图中涉及到的氧化物有 种
(2)将黄铁矿粉碎,目的是 .
(3)写出SO2转化为SO3的化学方程式 .
(4)炉渣(Fe2O3)在工业上可用来 .
(5)稀释浓硫酸的操作是 .

(1)流程图中涉及到的氧化物有
(2)将黄铁矿粉碎,目的是
(3)写出SO2转化为SO3的化学方程式
(4)炉渣(Fe2O3)在工业上可用来
(5)稀释浓硫酸的操作是
考点:物质的相互转化和制备,浓硫酸的性质及浓硫酸的稀释,从组成上识别氧化物,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:(1)根据氧化物是由两种元素组成,一种元素是氧元素的化合物进行分析;
(2)根据黄铁矿粉碎会增大反应物的接触面积加快反应速度进行分析;
(3)根据题中的反应流程分析反应物、生成物,然后依据质量守恒定律书写化学方程式;
(4)根据氧化铁可以用来炼铁进行分析;
(5)根据浓硫酸的稀释方法进行分析.
(2)根据黄铁矿粉碎会增大反应物的接触面积加快反应速度进行分析;
(3)根据题中的反应流程分析反应物、生成物,然后依据质量守恒定律书写化学方程式;
(4)根据氧化铁可以用来炼铁进行分析;
(5)根据浓硫酸的稀释方法进行分析.
解答:解::(1)氧化物是由两种元素组成,一种元素是氧元素,而流程中二氧化硫、三氧化硫、三氧化二铁满足氧化物的定义,所以涉及到的氧化物有三种;
(2)依据影响化学反应速率的因素可知,反应物接触面积越大,反应越剧烈,黄铁矿粉碎的目的是:增大反应物的接触面积,加快反应速率;
(3)二氧化硫和氧气在催化剂作用和加热的条件下生成三氧化硫,化学方程式是:2SO2+O2
2SO3;
(4)炉渣(Fe2O3)可以用来炼铁,一氧化碳与氧化铁反应生成铁和二氧化碳,所以可以用:做冶铁原料;(5)浓硫酸的稀释方法是:将浓硫酸沿着容器壁慢慢倒入水中,并用玻璃棒不断搅拌.
故答案为:(1)三种;
(2)增大反应物的接触面积,加快反应速率;
(3)2SO2+O2
2SO3;
(4)做冶铁原料;
(5)将浓硫酸沿着容器壁慢慢注入水中,并不断搅拌.
(2)依据影响化学反应速率的因素可知,反应物接触面积越大,反应越剧烈,黄铁矿粉碎的目的是:增大反应物的接触面积,加快反应速率;
(3)二氧化硫和氧气在催化剂作用和加热的条件下生成三氧化硫,化学方程式是:2SO2+O2
| ||
| △ |
(4)炉渣(Fe2O3)可以用来炼铁,一氧化碳与氧化铁反应生成铁和二氧化碳,所以可以用:做冶铁原料;(5)浓硫酸的稀释方法是:将浓硫酸沿着容器壁慢慢倒入水中,并用玻璃棒不断搅拌.
故答案为:(1)三种;
(2)增大反应物的接触面积,加快反应速率;
(3)2SO2+O2
| ||
| △ |
(4)做冶铁原料;
(5)将浓硫酸沿着容器壁慢慢注入水中,并不断搅拌.
点评:解答本题的关键是要知道氧化物的特点,知道反应物接触面积越大,反应越剧烈,熟悉化学方程式的书写注意事项,知道浓硫酸的稀释方法.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
已知:同温同压下,相同体积的任何气体所含分子数目相同.现将同温同压下的2L CO2和1L C2H2(乙炔)混合,所得混合气体中CO2和C2H2的分子数比是 ;混合气体中C、H、O三种元素的质量比是 .
下列化学实验操作的叙述中,正确的是.
| A、实验产生的废液应倒入指定的容器内 |
| B、用稀盐酸洗涤盛放过石灰水的试剂瓶 |
| C、浓硫酸不慎沾到皮肤上,应立即用氢氧化钠溶液冲洗 |
| D、用胶头滴管向容器中滴加试剂时,滴管应伸入容器中,以防滴到外面 |
| E、用白色点滴板代替试管,进行酸、碱溶液与指示剂反应的实验可节约药品 |
| F、称取5.0g氢氧化钠固体,必须放在左盘的称量纸上称量 |
以下实验方法不能达到目的是( )
| A、有食醋浸泡的方法,除去水壶中的水垢 |
| B、用锌粒和浓硫酸两种试剂制取干燥纯净的氢气 |
| C、用稀高锰酸钾溶液检测二氧化碳气体中是否含有二氧化硫气体 |
| D、向鸡蛋清溶液中加入少量浓硝酸并微热以检验蛋白质的存在 |

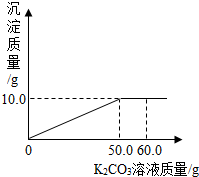 取KCl和CaCl2混合物15克,加入35克水完全溶解后,逐滴加入溶质质量分数为27.6%的K2CO3溶液,所加K2CO3溶液的质量的质量与生成沉淀质量的关系如图所示:
取KCl和CaCl2混合物15克,加入35克水完全溶解后,逐滴加入溶质质量分数为27.6%的K2CO3溶液,所加K2CO3溶液的质量的质量与生成沉淀质量的关系如图所示: 如图中A、B分别是某微粒的结构示意图,回答下列问题:
如图中A、B分别是某微粒的结构示意图,回答下列问题: