题目内容
已知:同温同压下,相同体积的任何气体所含分子数目相同.现将同温同压下的2L CO2和1L C2H2(乙炔)混合,所得混合气体中CO2和C2H2的分子数比是 ;混合气体中C、H、O三种元素的质量比是 .
考点:有关化学式的计算和推断,元素质量比的计算
专题:化学式的计算
分析:根据题意,同温同压下,相同体积的任何气体所含分子数目相同;则同温同压下的2L CO2和1L C2H2(乙炔)混合,混合气体中二氧化碳与乙炔的分子个数比为2:1,进而由二氧化碳与乙炔分子的构成、各元素质量比=各原子的相对原子质量×原子个数之比,计算混合气体中C、H、O三种元素的质量比.
解答:解:同温同压下,相同体积的任何气体所含分子数目相同;则同温同压下的2LCO2和1LC2H2(乙炔)混合,混合气体中二氧化碳与乙炔的分子个数比为2L:1L=2:1.
1个二氧化碳分子中含有1个碳原子和2个氧原子,1个乙炔分子中含有2个碳原子和2个氢原子,混合气体中C、H、O三种原子的原子个数比为(1×2+2):2:(2×
2)=4:2:4=2:1:2,则三种元素的质量比是(2×12):(1×1):(2×16)=24:1:32.
故答案为:2:1;24:1:32.
1个二氧化碳分子中含有1个碳原子和2个氧原子,1个乙炔分子中含有2个碳原子和2个氢原子,混合气体中C、H、O三种原子的原子个数比为(1×2+2):2:(2×
2)=4:2:4=2:1:2,则三种元素的质量比是(2×12):(1×1):(2×16)=24:1:32.
故答案为:2:1;24:1:32.
点评:本题难度不大,掌握同温同压下相同体积的任何气体所含分子数目相同、化学式的有关计算是正确解答本题的关键.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案
相关题目
下列说法正确的是( )
| A、50g水和50g酒精混合后,质量等于100g,符合质量守恒定律 |
| B、因为“质量守恒”,所以煤燃烧后产生的煤渣的质量一定和所用煤的质量相等 |
| C、铁丝在氧气中燃烧后,生成物的质量比铁丝的质量增加了 |
| D、铁能与氢氧化钠反应产生氢气 |
下列叙述与对应的示意图表示正确的是( )
A、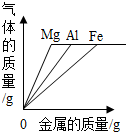 向三份等质量的相同的稀盐酸中分别加入等质量足量的镁、铝、铁 |
B、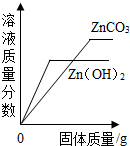 向等质量、等质量分数的两种稀硫酸中分别加入足量的Zn(OH)2和ZnCO3固体 |
C、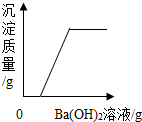 表示向盐酸和硫酸铜的混合溶液中加入Ba(OH)2溶液至过量 |
D、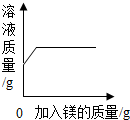 向一定质量的稀硫酸中加入镁至过量 |


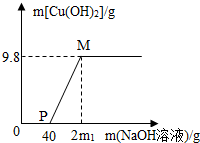 向含有CuCl2和HCl的混合溶液100g中,逐滴加入10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2.
向含有CuCl2和HCl的混合溶液100g中,逐滴加入10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2.