题目内容
以下实验方法不能达到目的是( )
| A、有食醋浸泡的方法,除去水壶中的水垢 |
| B、用锌粒和浓硫酸两种试剂制取干燥纯净的氢气 |
| C、用稀高锰酸钾溶液检测二氧化碳气体中是否含有二氧化硫气体 |
| D、向鸡蛋清溶液中加入少量浓硝酸并微热以检验蛋白质的存在 |
考点:酸的化学性质,常见气体的检验与除杂方法,氢气的制取和检验,鉴别淀粉、葡萄糖的方法与蛋白质的性质
专题:简单实验方案的设计与评价
分析:A、食醋中的醋酸能够和水垢中的碳酸钙反应,可以据此解答;
B、锌和浓硫酸不能制取氢气,可以据此解答;
C、根据高锰酸钾的强氧化性和二氧化硫的性质判断.
D、根据浓硝酸能和蛋白质发生反应使其变成黄色,热的酸能使蛋白质变性的性质回答
B、锌和浓硫酸不能制取氢气,可以据此解答;
C、根据高锰酸钾的强氧化性和二氧化硫的性质判断.
D、根据浓硝酸能和蛋白质发生反应使其变成黄色,热的酸能使蛋白质变性的性质回答
解答:解:A、食醋中的醋酸能够和水垢中的碳酸钙反应,所以可以用来除去水壶中的水垢,故A能达到目的;
B、浓硫酸具有强氧化性,所以锌和浓硫酸不能制取氢气,故B不能达到目的;
C、高锰酸钾有强氧化性,能被二氧化硫还原为无色物质,故C能达到目的;
D、浓硝酸能和蛋白质发生反应使其变成黄色,热的酸又能使蛋白质变性,所以在鸡蛋白中加浓硝酸,微热,观察到黄色沉淀的现象,故D能达到目的.
故选B.
B、浓硫酸具有强氧化性,所以锌和浓硫酸不能制取氢气,故B不能达到目的;
C、高锰酸钾有强氧化性,能被二氧化硫还原为无色物质,故C能达到目的;
D、浓硝酸能和蛋白质发生反应使其变成黄色,热的酸又能使蛋白质变性,所以在鸡蛋白中加浓硝酸,微热,观察到黄色沉淀的现象,故D能达到目的.
故选B.
点评:物质的检验是初中化学的难重点,也是中考的热点之一,了解物质的物理性质和化学性质,能运用比较法发现和利用物质间的性质差别是解题的关键.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
从小明同学整理的笔记中可以看出,不正确的一项是( )
| A、除去NaOH溶液中的Ca(OH)2杂质,加入适量Na2CO3溶液,过滤 |
| B、用熟石灰改良酸性土壤 |
| C、二氧化碳气体和氢气,分别通入紫色石蕊试液都变红色 |
| D、NaOH+HCl═NaCl+H2O,属于复分解反应 |
下列叙述与对应的示意图表示正确的是( )
A、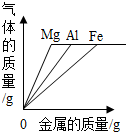 向三份等质量的相同的稀盐酸中分别加入等质量足量的镁、铝、铁 |
B、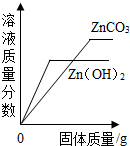 向等质量、等质量分数的两种稀硫酸中分别加入足量的Zn(OH)2和ZnCO3固体 |
C、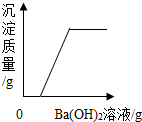 表示向盐酸和硫酸铜的混合溶液中加入Ba(OH)2溶液至过量 |
D、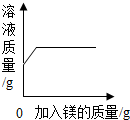 向一定质量的稀硫酸中加入镁至过量 |
染发时常用到的着色剂--对苯二胺,化学式为C6H8N2,是一种有毒化学药品,有致癌性,下列说法正确的是( )
| A、对苯二胺中含有N2分子 |
| B、对苯二胺中碳、氢、氮元素的质量比为6:8:2 |
| C、对苯二胺由6个碳原子、8个氢原子和2个氮原子组成 |
| D、对苯二胺中碳元素的质量分数为66.7% |
在进行化学实验探究时,认真操作、细心观察,可以培养我们严谨的科学态度.下列实验探究过程,可以明显感觉到溶于水有吸热现象的是( )
| A、食盐溶于水 |
| B、硝酸铵溶于水 |
| C、生石灰与水反应 |
| D、浓硫酸溶于水 |
下列有关水的说法正确的是( )
| A、水分子是保持水化学性质的最小微粒 |
| B、含有可溶性钙、镁化合物的水是硬水 |
| C、水、冰共融形成混合物 |
| D、电解水的实验证明水是由氢气和氧气组成的 |
如图所示,下列实验操作正确的是( )
A、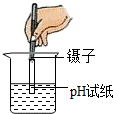 测定溶液的pH |
B、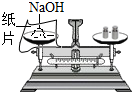 称量氢氧化钠 |
C、 稀释浓硫酸 |
D、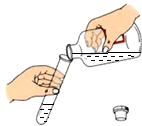 倾倒液体 倾倒液体 |
 如图是甲、乙两种固体物质的溶解度曲线,请据图回答下列问题.
如图是甲、乙两种固体物质的溶解度曲线,请据图回答下列问题.