题目内容
3.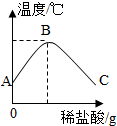 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,则下列说法错误的是( )
将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,则下列说法错误的是( )| A. | B点时,往烧杯中滴加无色酚酞试液,溶液变红色 | |
| B. | 从A到B过程中,烧杯中溶液的pH逐渐减小 | |
| C. | 稀盐酸与氢氧化钠溶液发生的反应是放热反应 | |
| D. | C点时烧杯中含有的溶质是NaCl、HCl |
分析 根据图象可以看出:随着盐酸的加入温度在逐渐上升,说明稀盐酸与氢氧化钠溶液发生的反应是放热反应;A到B的过程中温度逐渐升高,B点对于温度是个转折点,对于反应进程也是个转折点;B到C的过程的反应实质,加入的稀盐酸逐渐增多,稀盐酸过量,可以据此进行分析判断.
解答 解:A.根据图象可以看出,随着稀盐酸的加入,温度逐渐升高,在B点前后温度是两种情况,B点温度最高,B点表示酸碱恰好完全反应,反应后生成氯化钠和水,显中性,滴加无色酚酞试液不变色,故选项说法错误.
B.由图是可知,从A到B过程中,氢氧化钠逐渐减少,碱性减弱,故pH值逐渐减小,故选项说法正确.
C.图象可以看出:随着盐酸的加入温度在逐渐上升,说明稀盐酸与氢氧化钠溶液发生的反应是放热反应,故选项说法正确.
D.到C的过程中,是盐酸完全中和完氢氧化钠后继续加入稀盐酸,稀盐酸过量,故溶液中的溶质含有NaCl和HCl,故选项说法正确.
故选A.
点评 本题难度不是很大,本题主要考查了结合图象考查了中和反应的应用,理解图象的含义、掌握中和反应的实质是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.氧气是人类生产生活的重要资源.下列关于氧气的叙述中错误的是( )
| A. | 动植物的呼吸离不开它 | B. | 不易溶于水 | ||
| C. | 具有氧化性,是一种常用的氧化剂 | D. | 能够燃烧 |
18. 已知氯化钠、碳酸钠在不同温度时的溶解度如下:
已知氯化钠、碳酸钠在不同温度时的溶解度如下:
(1)依据上表数据,绘制出了氯化钠和碳酸钠的溶解度曲线(如图),图中能表示碳酸钠溶解度曲线的是A(填“A”或“B”).
(2)图中两溶解度曲线相交于M点,此点表示的意义是30℃时,A和B的溶解度相等.
(3)40℃时,把50g A物质放入100g水中,充分搅拌,所得溶液是溶液饱和(填“饱和”或“不饱和”).
(4)生活在盐湖(主要成分是NaCl和Na2CO3)附近的人们习惯“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”.请你答出“冬天捞碱”的道理碳酸钠的溶解度受温度变化影响较大,温度低时,溶解度较小,温度高时,溶解度较大,冬天温度降低,碳酸钠溶解度较小,会结晶析出.
 已知氯化钠、碳酸钠在不同温度时的溶解度如下:
已知氯化钠、碳酸钠在不同温度时的溶解度如下:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35 | 35.5 | 36 | 36.5 | 37 |
| 碳酸钠 | 6 | 10 | 18 | 36.5 | 50 | |
(2)图中两溶解度曲线相交于M点,此点表示的意义是30℃时,A和B的溶解度相等.
(3)40℃时,把50g A物质放入100g水中,充分搅拌,所得溶液是溶液饱和(填“饱和”或“不饱和”).
(4)生活在盐湖(主要成分是NaCl和Na2CO3)附近的人们习惯“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”.请你答出“冬天捞碱”的道理碳酸钠的溶解度受温度变化影响较大,温度低时,溶解度较小,温度高时,溶解度较大,冬天温度降低,碳酸钠溶解度较小,会结晶析出.
12. PX:无色透明液体,具有芳香气味,能与乙醇等有机溶剂混溶,可燃,低毒,毒性略高于乙醇,其蒸气与空气可形成爆炸性混合物.如图是“PX”的结构模型,下列有关“PX”的说法不正确的是( )
PX:无色透明液体,具有芳香气味,能与乙醇等有机溶剂混溶,可燃,低毒,毒性略高于乙醇,其蒸气与空气可形成爆炸性混合物.如图是“PX”的结构模型,下列有关“PX”的说法不正确的是( )
 PX:无色透明液体,具有芳香气味,能与乙醇等有机溶剂混溶,可燃,低毒,毒性略高于乙醇,其蒸气与空气可形成爆炸性混合物.如图是“PX”的结构模型,下列有关“PX”的说法不正确的是( )
PX:无色透明液体,具有芳香气味,能与乙醇等有机溶剂混溶,可燃,低毒,毒性略高于乙醇,其蒸气与空气可形成爆炸性混合物.如图是“PX”的结构模型,下列有关“PX”的说法不正确的是( )| A. | “PX”属于有机化合物 | |
| B. | “PX”可燃,低毒都属于它的化学性质 | |
| C. | “PX”中含有8个碳原子、10个氢原子 | |
| D. | “PX”中C、H两种元素的质量比为48:5 |
13.“端午节”前,质监部门对市场上的粽叶进行专项检查时,发现有些颜色翠绿的粽叶是用硫酸铜溶液浸泡的,人吃了用这种粽叶包的粽子,严重影响身体健康.但硫酸铜在农业上可用于配制农药--波尔多液.可见,合理利用化学物质可以造福于人类,反之则会给人类带来危害.请回答:
(1)配制硫酸铜溶液常常用到胆矾晶体,它的化学式为CuSO4•5H2O.
(2)农业上配制成的波尔多液不能用金属铝罐盛放,试用化学方程式进行解释2Al+3CuSO4=Al2(SO4)3+3Cu.
(3)测量人体血液密度的方法是:在几只试管内分别装有密度不同的硫酸铜溶液,然后向每支试管中分别滴入一滴血液,分析人员只要看到某个玻璃管中的血液呈悬浮状态就能知道血液的密度.
(4)如图是某同学为测定胆矾中结晶水质量分数的主要实验步骤示意图:

实验中称量得到如下数据:
胆矾中结晶水的质量分数的计算公式可表示为:w (H2O)=$\frac{{m}_{3}-{m}_{2}}{{m}_{2}-{m}_{1}}×100%$(请用字母表示);实验过程中,下列操作会使结晶水的质量分数w (H2O)计算值偏小的是AD.
A.加热后坩埚放在空气中冷却 B.加热时搅拌不当使晶体溅出坩埚外
C.加热温度过高,最终坩埚中固体部分变黑 D.晶体尚带蓝色,即停止加热.
(1)配制硫酸铜溶液常常用到胆矾晶体,它的化学式为CuSO4•5H2O.
(2)农业上配制成的波尔多液不能用金属铝罐盛放,试用化学方程式进行解释2Al+3CuSO4=Al2(SO4)3+3Cu.
(3)测量人体血液密度的方法是:在几只试管内分别装有密度不同的硫酸铜溶液,然后向每支试管中分别滴入一滴血液,分析人员只要看到某个玻璃管中的血液呈悬浮状态就能知道血液的密度.
(4)如图是某同学为测定胆矾中结晶水质量分数的主要实验步骤示意图:

实验中称量得到如下数据:
| 加热前坩埚的质量/g | 加热后坩埚的总质量/g | |
| m1(坩埚) | m2(坩埚+晶体) | m3 |
A.加热后坩埚放在空气中冷却 B.加热时搅拌不当使晶体溅出坩埚外
C.加热温度过高,最终坩埚中固体部分变黑 D.晶体尚带蓝色,即停止加热.
 如图所示,“→”表示由一种物质转化为另一种物质,“--”表示两种物质间可以反应,其他的生成物略去.A--F都是初中化学中常见的物质,其中A是常用作建筑材料,D是人体胃液中的一种成分,E、F都是氧化物,请判断:
如图所示,“→”表示由一种物质转化为另一种物质,“--”表示两种物质间可以反应,其他的生成物略去.A--F都是初中化学中常见的物质,其中A是常用作建筑材料,D是人体胃液中的一种成分,E、F都是氧化物,请判断: 在做完“用稀盐酸和石灰石反应制取二氧化碳”的试验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验.
在做完“用稀盐酸和石灰石反应制取二氧化碳”的试验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验.